随着国家层面仿制药一致性评价政策的逐步明确,配套政策的不断出台,以及以入围资格通过仿制药一致性评价的药品集采活动“47”的实施,越来越多的企业意识到,只要想保住相关品种的一定市场份额,仿制药一致性评价就是一道绕不过去的坎,越早开展越有利于后续的市场进攻。
那么,到目前为止,仿制药一致性评价的应用现状如何?通过的品种有哪些?下面我们就和GBISOURCE数据库一起回顾一下2019年4月仿制药一致性评价的具体进展。
一、2019年4月新增通过仿制药一致性评价品规
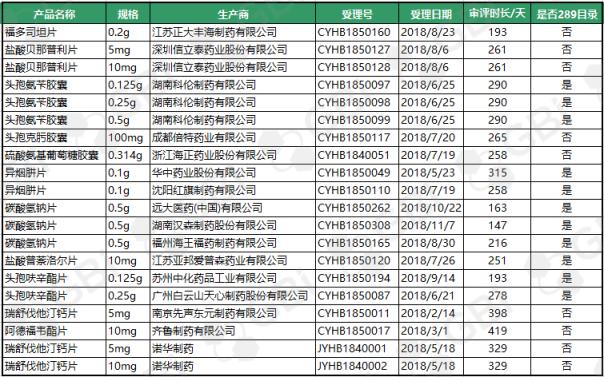
截至2019年4月29日,4月份有20个新品规格通过仿制药一致性评价。其中11个规格为289个目录品种。此外,诺华子公司乐克的瑞舒伐他汀钙片(5mg、10mg)以“通过质量和疗效一致性评价的药品”的名义被《中国上市药品目录集》采集,这意味着诺华瑞舒伐他汀顺利通过一致性评价,成为首个通过一致性评价的进口仿制药。
二、2019年4月新增视同通过仿制药一致性评价品规
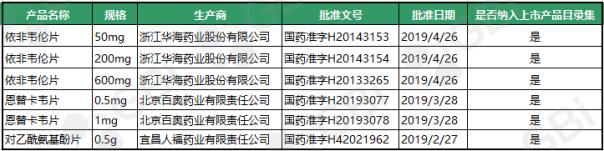
根据GBI来源数据库,截至2019年4月29日,4月新增6个产品,均被视为通过仿制药一致性评价。目前已全部支付《中国上市药品目录集》。根据华海药业的公告,2018年12月29日,国家美国食品药品监督管理局发布《仿制药参比制剂目录(第十九批)的通告(2018年第135号)》,华海药业生产的依法韦仑片(规格:50mg、200mg、600mg)因“原研技术转让”被列入其中。近日,依法韦仑片正式进入《中国上市药品目录集》,这标志着依法韦仑片已经通过仿制药。
三、仿制药一致性评价通过企业达3家及以上品规
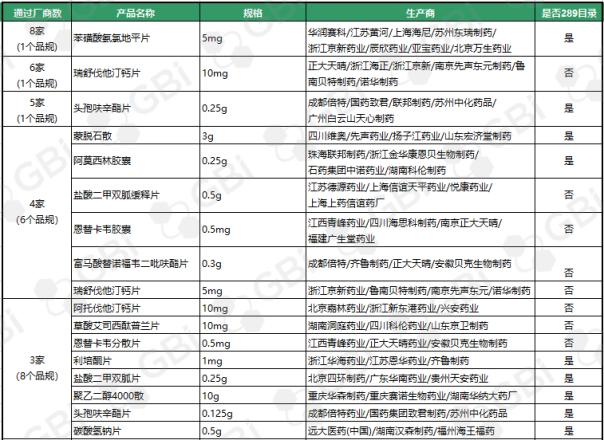
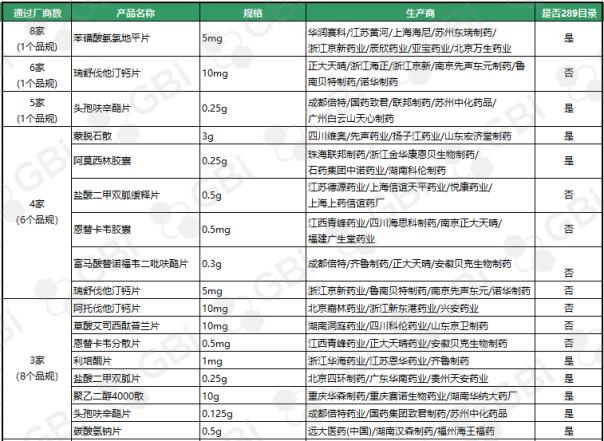
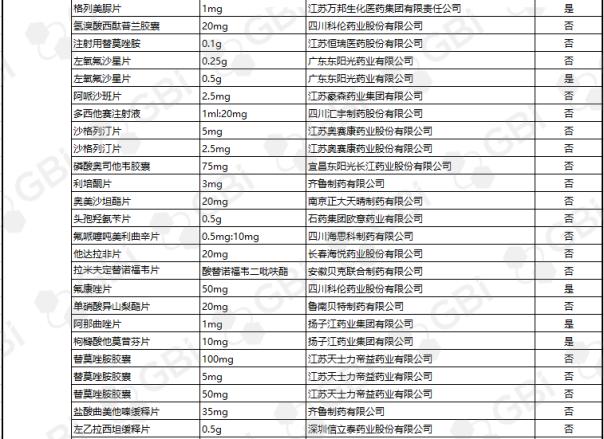
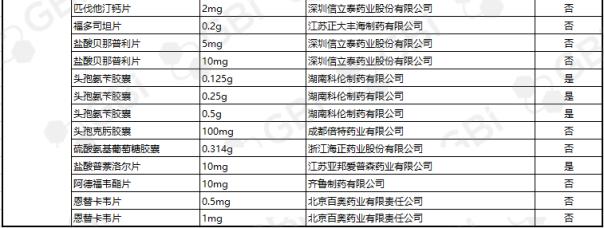
截至目前,通过仿制药一致性评价或被视为通过仿制药一致性评价的企业达到3家及以上,共17个产品。其中苯磺酸氨氯地平片(5mg)有8家企业获批;利伐他汀钙片(10mg)获6家企业批准;头孢呋辛酯片(0.25g)获5家企业批准;蒙脱石散(3g)、阿莫西林胶囊(0.25g)、盐酸二甲双胍缓释片(0.5g)、恩替卡韦胶囊(0.5 mg)、富马酸替诺福韦酯片(0.3g)、瑞舒伐他汀钙片(5 mg)。目前,已有4家企业通过了仿制药一致性评价。3家企业通过的8个产品规格分别是:阿托伐他汀钙片(10mg)、草酸艾司西酞普兰片(10mg)、恩替卡韦分散片(0.5 mg)、利培酮片(1mg)、盐酸二甲双胍片(0.25g)、聚乙二醇4000粉末(10g)、头孢呋辛酯片(0.125g
四、仿制药一致性评价总体进展
GBI源数据库显示,截至2019年4月29日,CDE仿制药一致性评价累计受理数量已达1082件,涉及341家企业的266个品种。目前已有245个产品法规通过或被视为通过了仿制药一致性评价。其中,1项产品规格已通过8家企业;一项产品规格已通过6家企业;一项产品规格已通过5家企业;六种产品经过四家企业;8个产品通过了3家企业;21项产品规格已通过2家企业;有一家企业通过了36项产品规范(详细列表见下表)。
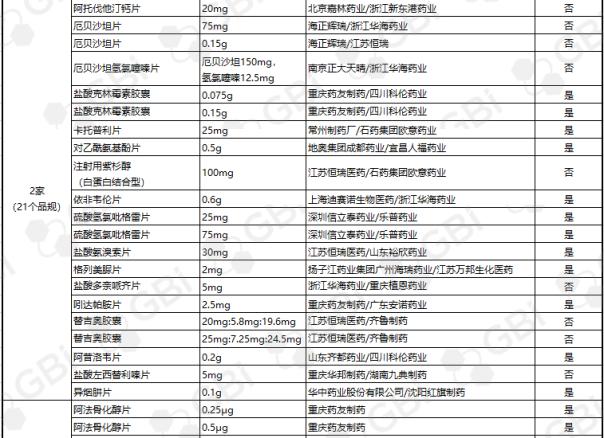
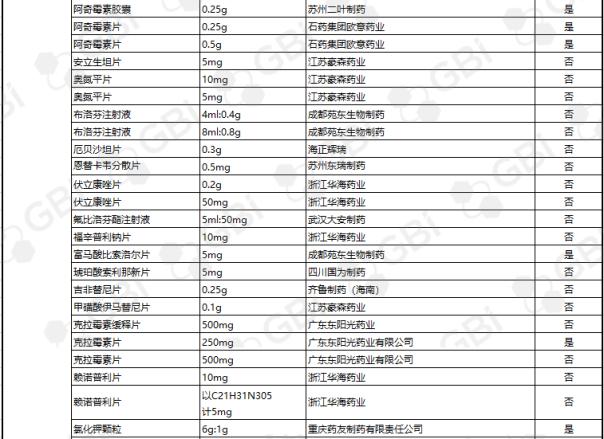
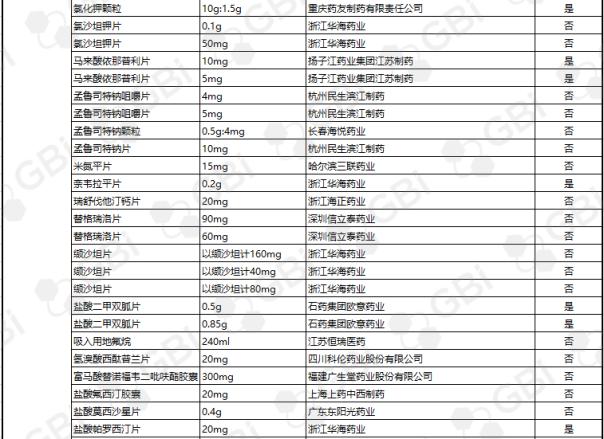
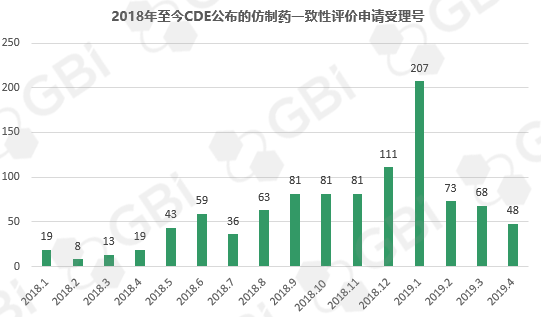
五、2018年至今CDE受理仿制药一致性评价变化趋势
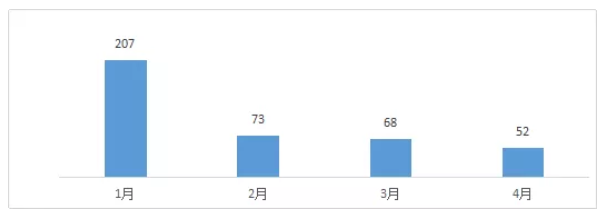
根据GBI源数据库【药品申报统计】工具统计结果,2019年4月,CDE新受理仿制药一致性评价申请48件(数据统计截至4月29日)。从审批节奏来看,目前仿制药一致性评价已经进入密集收获期。2019年1月,CDE共接受了207份申请,创下新高,但随后步伐放缓,2月、3月和4月分别有73份、68份和48份申请。
4月25日,在国家卫健委召开的“深化医药领域改革典型经验新闻发布会”上,国家卫健委机构改革司副司长薛海宁表示,“加快仿制药质量和疗效一致性评价,是推动我们从医药大国向医药强国跨越的一个非常重要的举措。要落实仿制药相关支持和激励政策,支持仿制药替代使用。“业内人士表示,无论是从政策层面还是市场层面,趋势都非常明确:没有通过一致性评价的品种将被迅速淘汰,而原研产品与通过一致性评价的品种之间的竞争将迅速升级。仿制药对原研产品的替代正在形成,并将继续下去。降价和控费仍将是中国医药行业长期的主旋律。