自2017年首个CAR-T疗法上市以来,全球已有5个CD19 CAR-T和1个BCMA CAR-T疗法获得批准。累积适应症包括急性淋巴细胞白血病、弥漫性大B细胞淋巴瘤、原发性纵隔B细胞淋巴瘤、套细胞淋巴瘤、滤泡性淋巴瘤和多发性骨髓瘤。然而,尽管CAR-T细胞疗法已被证明是对抗恶性血液肿瘤的有力武器(有些病例在接受治疗后多年仍保持无癌状态),但这种疗法在治疗实体肿瘤方面的效果要差得多,部分原因是CAR-T在重新注入患者体内后会经历一个称为“衰竭(功能障碍)”的过程。
T细胞耗竭的现象被认为是为了防止这些强大的免疫细胞对身体造成过多的附带损害。当T细胞与靶抗原接触时间过长(约数周)时,就会触发耗竭过程,这也是实体肿瘤微环境中的典型情况。
12月2日,在最近发表在《细胞》杂志上的一项研究中,来自宾夕法尼亚大学佩雷尔曼医学院的科学家团队揭示了CAR-T耗竭过程的关键分子机制,并指出了克服耗竭过程的潜在有效策略,为CAR-T治疗实体肿瘤带来了新的希望。CAR-T的先驱Carl H. June教授是这篇论文的合著者之一。
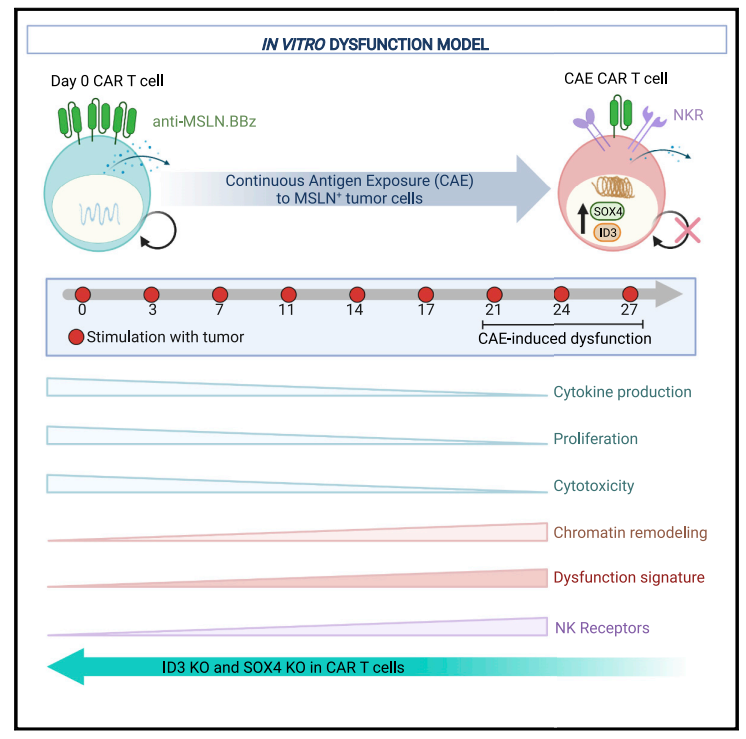
在这项研究中,卡尔教授。June和他的同事开发了一个实验室培养皿模型,使他们能够全面研究用于攻击胰腺肿瘤的CAR-T细胞的耗竭过程。发现遗传调节因子ID3和SOX4在T细胞耗竭过程中起关键作用,沉默这两个因子大大增强了CAR-T杀伤肿瘤的效果。
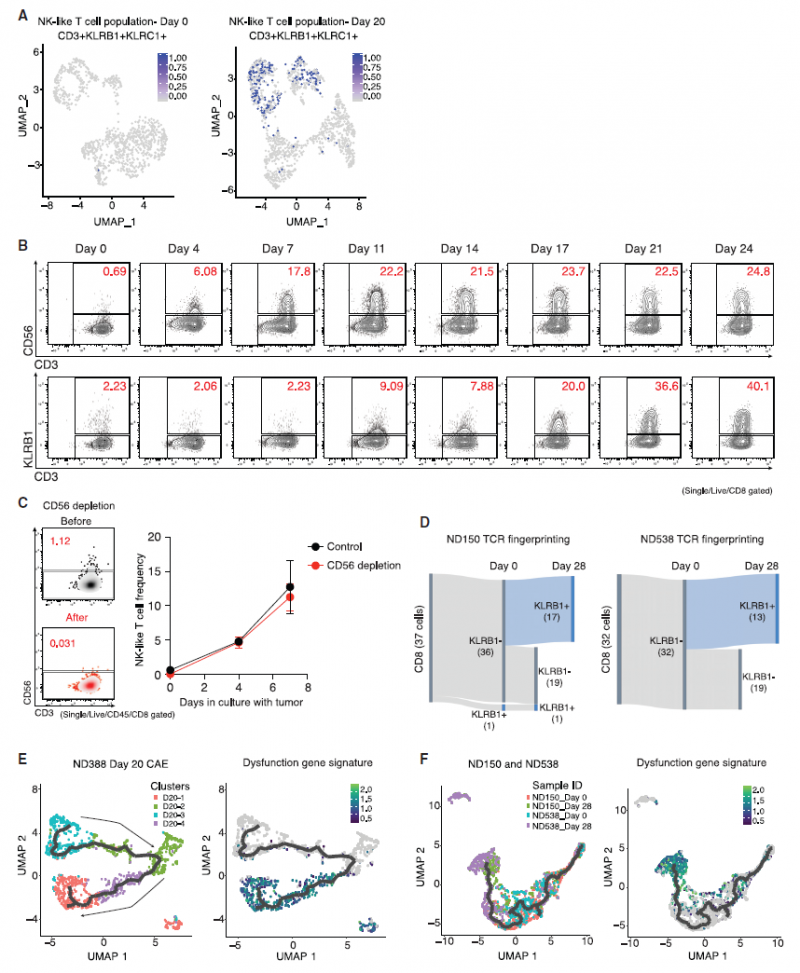
在抗原的持续刺激下,CD8 T细胞转化为NK样T细胞(来源:细胞)
具体来说,他们设计了一种靶向CAR-T细胞的间皮素,并将CAR-T细胞暴露于表达间皮素的胰腺肿瘤细胞4周。分析表明,CAR-T细胞不仅表现出一些典型的衰竭迹象,还出现了一些以前研究中不明显的变化,如T细胞身份的一些变化:从T细胞部分转化为NK细胞。科学家还在癌症患者衰竭的CAR-T细胞中发现了T细胞转化为NK细胞的类似迹象。
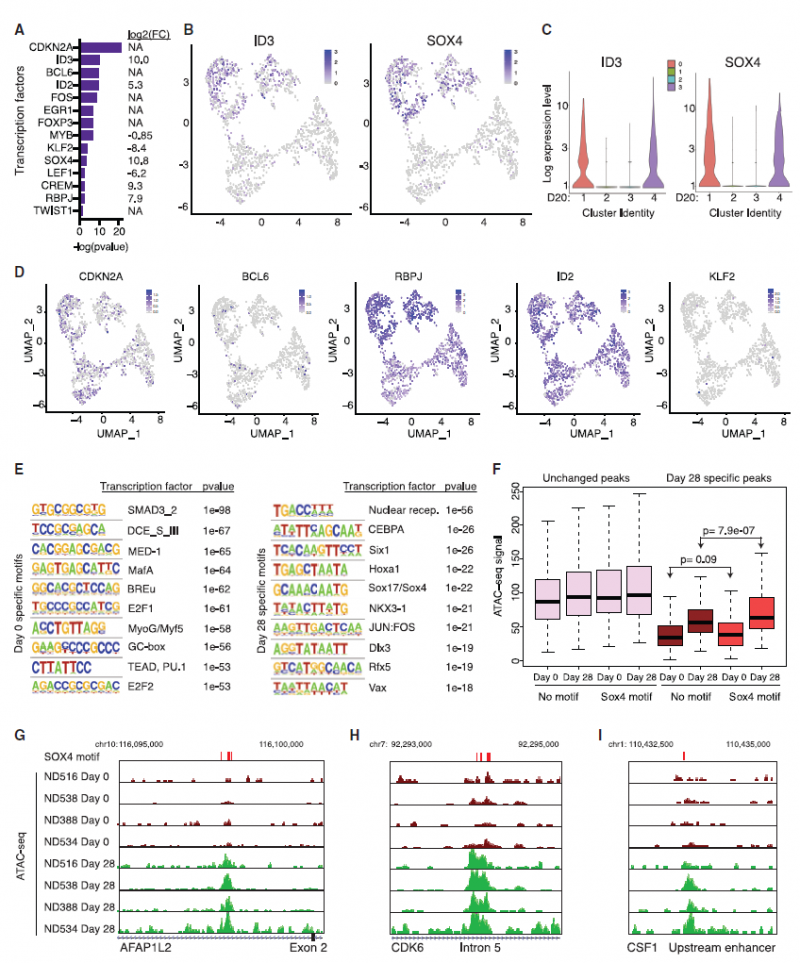
ID3和SOX4是功能障碍(衰竭)的潜在调节剂(来源:细胞)
更重要的是,研究人员观察到,CAR-T细胞的衰竭伴随着ID3和SOX4水平的急剧增加,这是免疫细胞中大量基因的主要开关。研究表明,沉默这些明显的T细胞耗竭开关可以使耗竭的CAR-T细胞在长期接触肿瘤细胞后保持其肿瘤杀伤效应。这些发现表明,抑制ID3和/或SOX4可能有助于CAR-T细胞更好地对抗实体瘤。
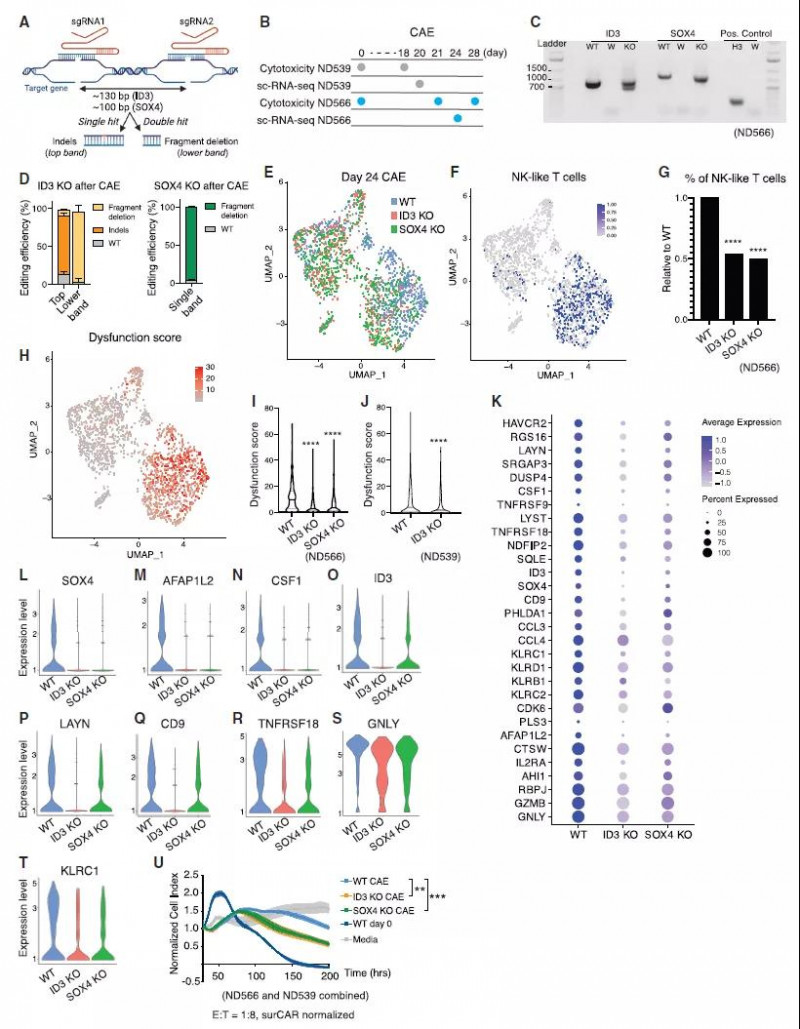
ID3和SOX4的破坏改善了CAR-T的效应功能(来源:细胞)
总之,本研究揭示了人CAR-T细胞的可塑性,并证明下调ID3和SOX4的表达可以通过预防或延缓CAR-T细胞的功能障碍来提高CAR-T细胞对实体瘤的治疗效果。
注:原文已删除。
参考资料:
[1] Charly R. Good等.一种NK样CAR T细胞转变中的CAR T细胞功能障碍。单元格(2021)。
[2]研究发现,对t细胞衰竭的新认识可以改善癌症免疫疗法(来源:宾夕法尼亚大学佩雷尔曼医学院)
