为加强医疗器械临床试验的监督管理,指导监管部门开展医疗器械临床试验的监督检查工作,根据《医疗器械注册管理办法》和《医疗器械临床试验质量管理规范》的要求,国家医疗用品管理局近日组织制定了《医疗器械临床试验检查要点及判定原则》。
医疗器械临床试验检查要点及判定原则
根据《医疗器械注册管理办法》和《医疗器械临床试验质量管理规范》的要求,制定检查要点和判定原则,用于指导医疗器械临床试验现场检查。
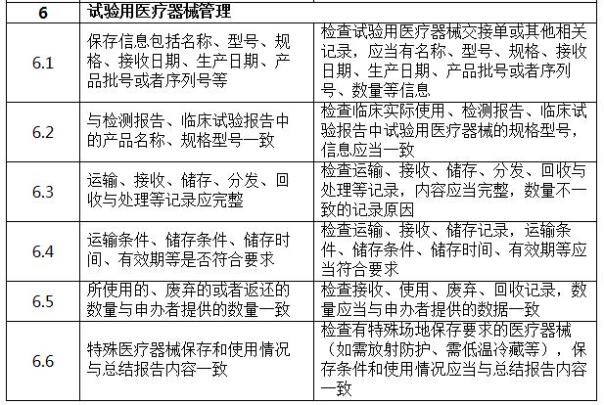
一、检查要点
二、判断原则
根据检查中发现的问题,按照以下原则判断检查结果:
(1)有下列情形之一的,判定真实性有问题:
1.编造受试者信息、主要试验过程记录、研究数据、试验数据等临床试验数据。影响医疗器械安全性和有效性的评价结果;
2.排除标准、主要疗效指标、重要安全性指标等临床试验数据无法追溯;
3.实验医疗器械不真实,如以对照医疗器械代替实验医疗器械、以实验医疗器械代替对照医疗器械、以其他方式使用虚假实验医疗器械等;
4.隐瞒与临床试验中使用的医疗器械有关的严重不良事件以及可能导致严重不良事件中医疗器械存在缺陷的药物或者医疗器械的组合以及禁止使用计划的;
5.注册申请的临床试验报告中的数据与临床试验机构保存的临床试验报告中的数据不一致,影响医疗器械安全性和有效性评价结果的;
6.申请注册的临床试验统计分析报告中的数据与临床试验统计数据库或分中心临床试验总结中的数据不一致,影响医疗器械安全性和有效性评价结果的;
7.故意破坏医疗器械临床试验数据真实性的其他情形。
(2)未发现真实性问题,但临床试验过程不符合《医疗器械临床试验相关规范》要求的,判定存在合规性问题。
(3)如未发现上述问题,则判定为符合要求。