9月20驲正在CSCO年会上,上海复星医药控股子公司复宏汉霖自立研发的生物近似药利妥昔单抗(HLX-01)颁布要害3期临床数据,HLX-01与原研药(美罗华)正在医治CD20阳性弥漫型年夜B非霍奇金淋巴瘤初治患者的临床试验次要尽头、主要尽头(安全性、免疫原性、药代动力学)均到达预设尺度。HLX-01是现阶段独一一个处于上市审评阶段的利妥昔单抗生物近似药。
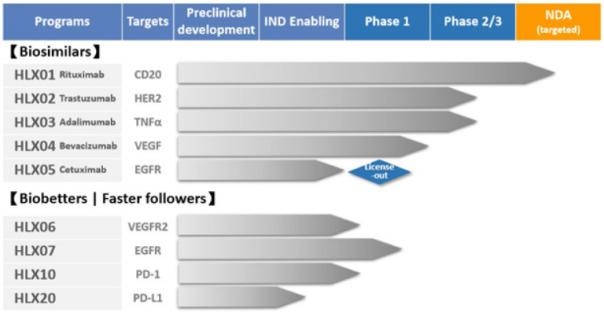
笔者汇总了HLX-01跟原研药正在DLBCL适应症的临床数据,并借助此文剖析了现阶段海内CD20单抗的开辟跟注册申报希望。
1、首款海内自立研发利妥昔单抗HLX-01行将上市
2017年10月30驲,CFDA受理复宏汉霖HLX-01上市请求(CXSS1700026)该审评归入第26批优先审评目次,现阶段该产物已实现技巧审评跟三合一审评。除弥漫性年夜B细胞淋巴瘤适应症中,类风湿关节炎处于3期临床。
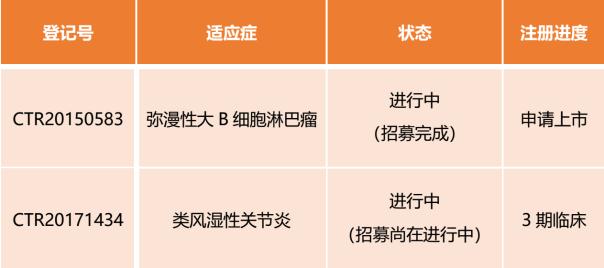
2018年09月20驲,CSCO年会上,上海复星医药控股子公司复宏汉霖自立研发的HLX-01颁布要害3期临床数据。
要害3期临床数据:HLX-01的3期临床研讨是一项随机、双盲、平行对比的多中间(33家)临床试验(CTR20150583,NCT02787239),该研讨招募患者407例,评估生物近似药与原研药作为弥漫型年夜B非霍奇金淋巴瘤一线疗法的安全性跟有效性。
利妥昔单抗注射液与原研药(美罗华)正在医治CD20阳性弥漫型年夜B非霍奇金淋巴瘤初治患者的临床试验次要尽头、主要尽头(安全性、免疫原性、药代动力学)均到达预设尺度。
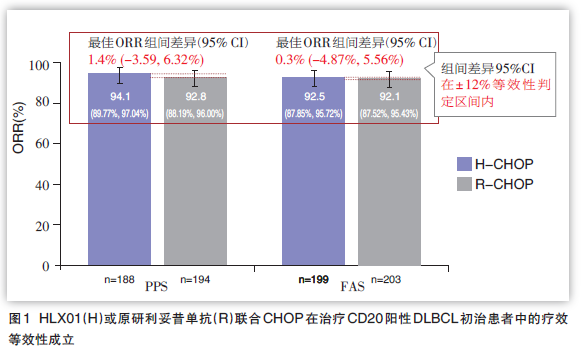
揭盲后疗效成果图表
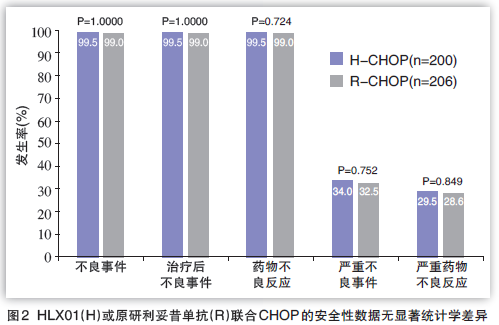
揭盲后安全性成果图表
2、海内CD20单抗药物汇总剖析
笔者依据公然渠道,收拾整顿了现阶段海内正在注册申报的CD20单抗药物,此中,海内已上市2款,原研产物罗氏美罗华(利妥昔单抗)海内已上市18年;三生国健利妥昔单抗生物近似药曾报产(撤回),5款处于3期临床,9款处于1期临床。
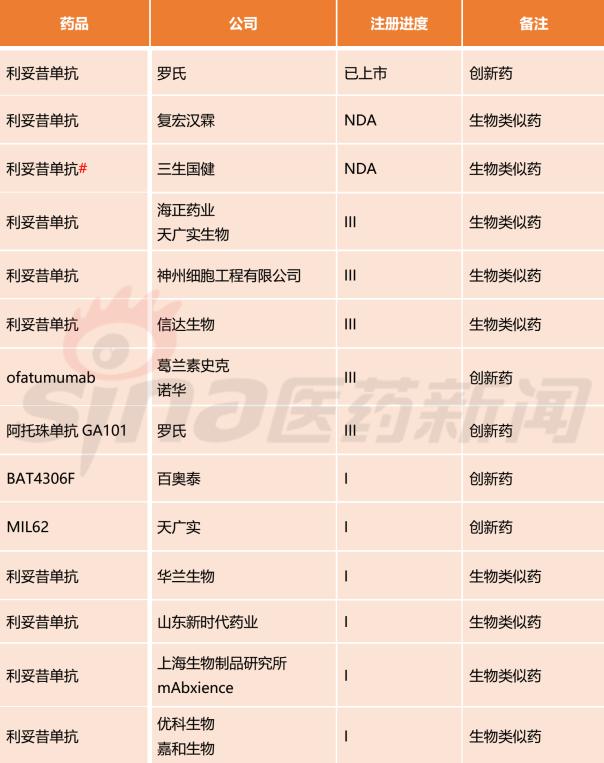
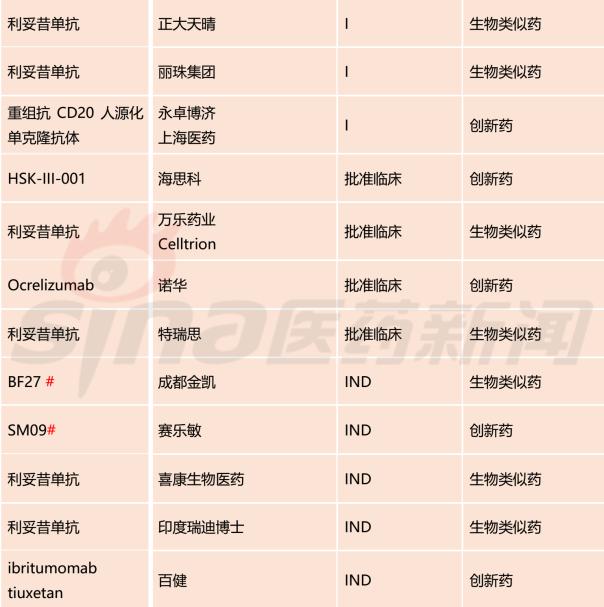
备注:#为自动撤回
海内正在申报的CD20单抗25款种类中,生物近似药16款,翻新药9款,笔者正在这里不再比照各翻新药的序列差别,行业内读者可以对相关抗体做更加深化的剖析,如9款抗体药物的要害数据,包罗安全性、免疫原性跟临床有效性数据。
远段时间,国产抗体生物近似药连续报,虽然中国生物近似药上市的工夫晚于欧盟跟美国多年,可是,首款美罗华的上市将依旧意思不凡。
2017年医保准入会谈后,利妥昔单抗500mg/50ml的价钱为8290元人民币,贬价幅度高达58.45%,年用度正在18.6万人民币。
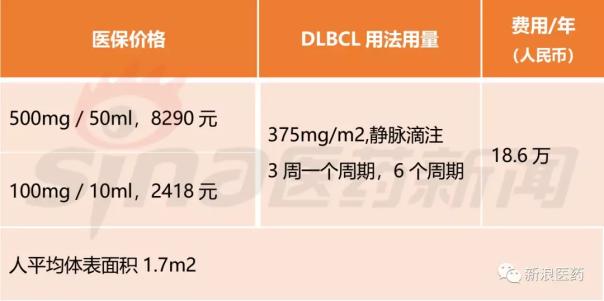
那么,国产美罗华将会若何订价?迎接留言交换。