6月20日,根据《关于加快落实仿制药供应保障及使用政策工作方案》等文件精神要求,卫健委药政司正式公示《第一批鼓励仿制药品目录建议清单》。根据此前公布的《方案》,加快提升上市药品质量。自2020年起,每年年底前公布鼓励仿制的药品目录,目录内药品享受一系列优惠政策。这也意味着国家正在采取实际行动鼓励和引导仿制药产业的发展。
那么,到目前为止,仿制药一致性评价的应用现状如何?6月份新采用的品种有哪些?下面就和GBI源数据库一起回顾一下2019年6月仿制药一致性评价的具体进展。
一、2019年6月新增通过仿制药一致性评价品规
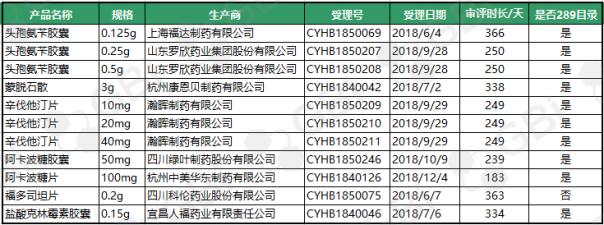
截至2019年6月26日,6月份有11个新产品通过仿制药一致性评价。其中10个规格为289个目录品种。
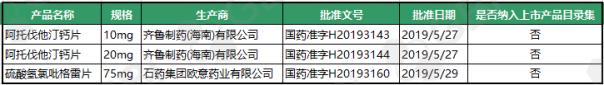
二、2019年6月新增视同通过仿制药一致性评价品规
根据GBSource GBiSource的数据库,截至2019年6月26日,6月新增3个产品,均被视为通过仿制药一致性评价。目前都没有被纳入《中国上市药品目录集》。
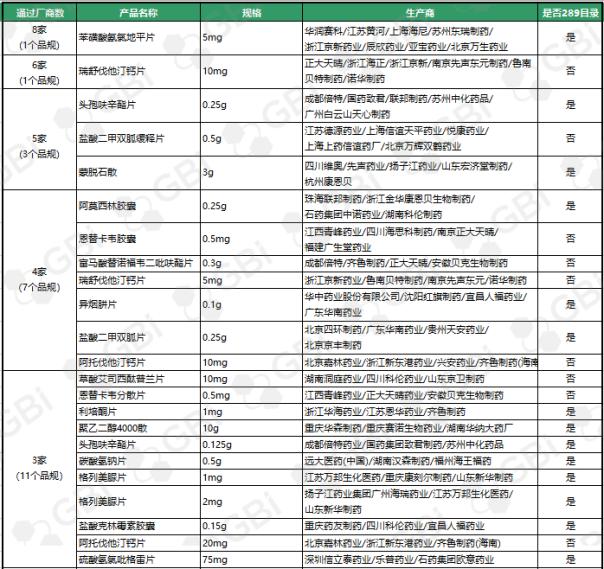
三、仿制药一致性评价通过企业达3家及以上品规
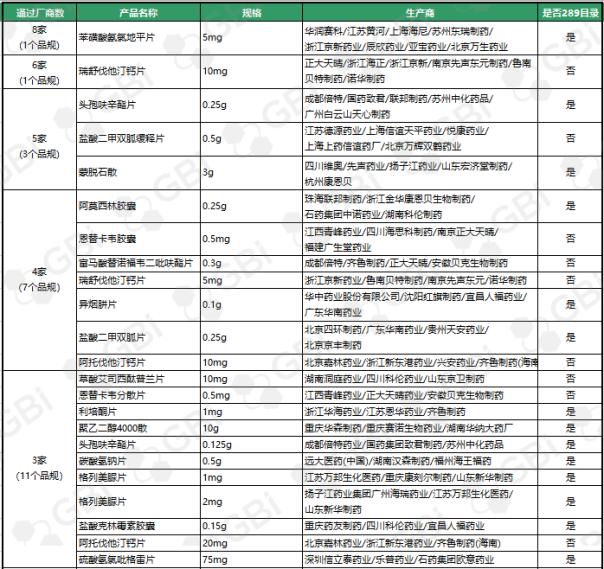
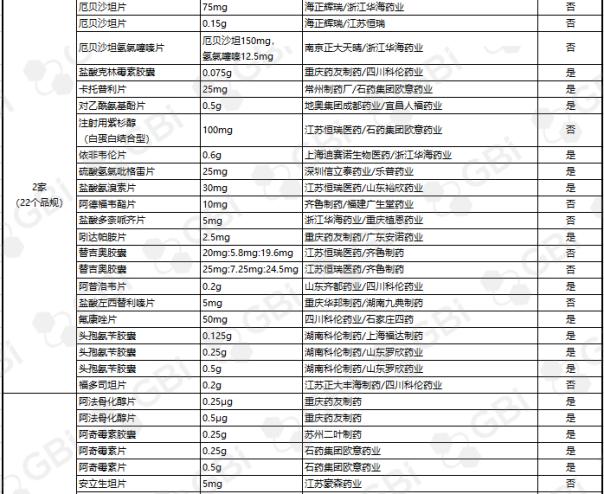
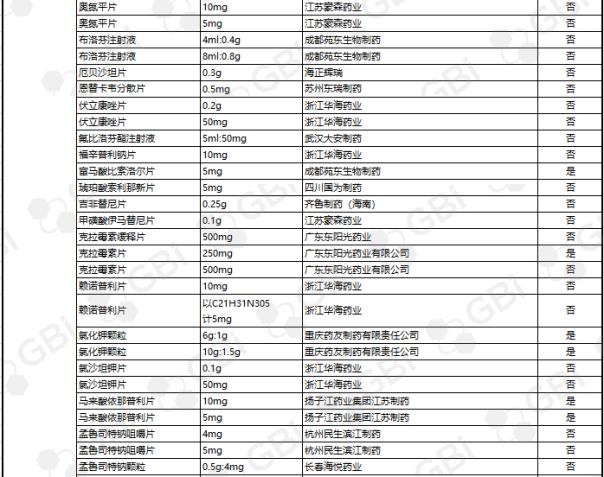
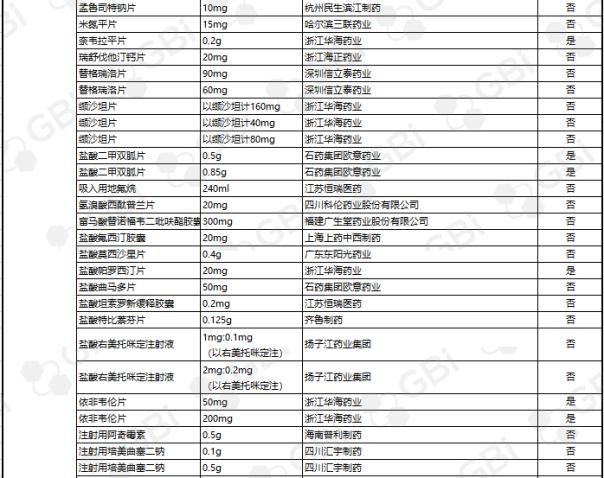
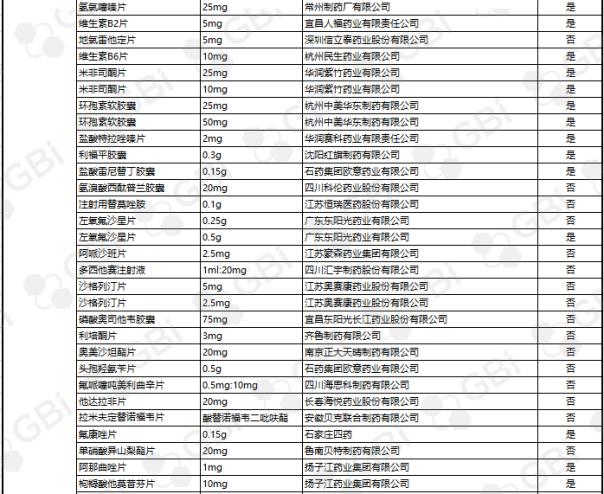
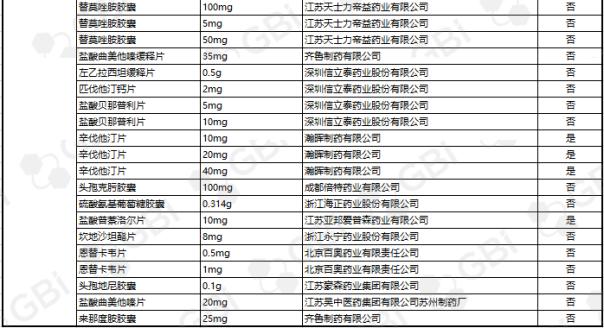
截至目前,通过仿制药一致性评价或被视为通过仿制药一致性评价的企业达到3家及以上,共23个产品。其中苯磺酸氨氯地平片(5mg)有8家企业获批;利伐他汀钙片(10mg)获6家企业批准;头孢呋辛酯片(0.25g)、盐酸二甲双胍缓释片(0.5g)、蒙脱石散(3g)5家企业获批;阿莫西林胶囊(0.25g)、恩替卡韦胶囊(0.5 mg)、富马酸替诺福韦酯片(0.3g)、瑞舒伐他汀钙片(5 mg)、异烟肼片(0.1g)、盐酸二甲双胍片(0.25g)、阿托伐他汀钙片(10mg)4家企业通过仿制药一致性。3家企业通过的11个产品规格分别是草酸艾司西酞普兰片(20mg)、恩替卡韦分散片(0.5 mg)、利培酮片(1mg)、聚乙二醇4000粉(10g)、头孢呋辛酯片(0.125g)、碳酸氢钠片(0.5g)、格列美脲片(1mg
四、仿制药一致性评价总体进展
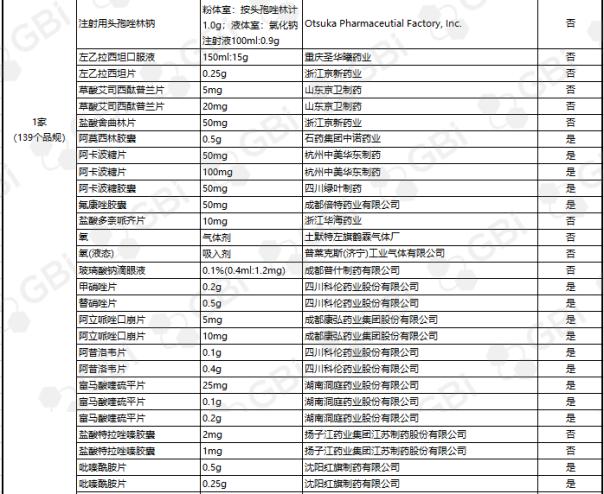
GBI源数据库显示,截至2019年6月26日,CDE仿制药一致性评价累计受理数量已达1207件,涉及368家企业的282个品种。目前已有273个产品法规通过或被视为通过了仿制药一致性评价。其中,1项产品规格已通过8家企业;一项产品规格已通过6家企业;三种产品规格经过五家企业;七种产品规格,经过四家企业;1产品规格通过3家企业;两个产品经过了两个企业;有一家企业通过了39项产品规范(详细清单见下表)。
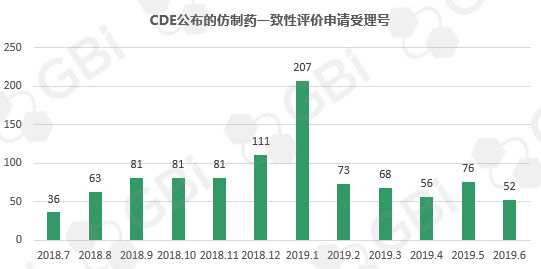
五、CDE受理仿制药一致性评价变化趋势
GBI源数据库【药品申报统计】工具统计结果显示,2019年6月,CDE新受理仿制药一致性评价申请52件(数据统计截至6月26日),较5月无明显增加。
近日,随着中印药品监管交流会的召开,有业内人士推测,来自仿制药大国印度的药企进入中国抢占市场的进程可能会加快。印度进入本土市场,无疑将迫使本土仿制药成为刺激本土仿制药产业升级的动力之一,以巩固市场,提高质量,降低价格。同时,印度仿制药一旦放开进入中国市场,将给中国仿制药行业和企业带来更大压力。