今天,Verastem公司宣布,它已向FDA提交了领先候选药物duvelisib的上市申请。Verastem预计,这种新药将被完全批准用于治疗复发性或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤,并加速用于治疗复发性或难治性滤泡性淋巴瘤。

Duvelisib是正在开发的同类新药中的第一个,它可以同时抑制PI3K-和PI3K-。这两种酶在恶性B细胞和T细胞的生长和存活中起着关键作用:它们的信号通路可以引起恶性B细胞和T细胞的增殖,也可能在肿瘤微环境的形成和维持中起作用。作为一种具有创新机制的新药,研究人员正在多个临床试验中评估duvelisib的疗效。基于临床试验证明的积极结果,duvelisib已获得FDA颁发的快速通道资格和孤儿药资格。
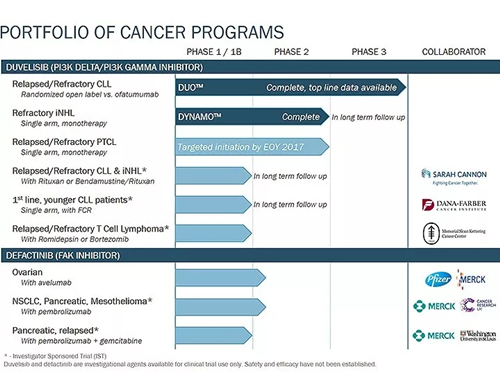
在名为DUO的3期临床试验中,duvelisib的有效性和安全性得到了进一步验证。该试验招募了患有复发性或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤的患者,并使用duvelisib作为单一药物对他们进行治疗。结果显示,与使用ofatumumab的对照组相比,使用duvelisib治疗的患者的无进展生存期(PFS)在统计学上显著延长(中位PFS PFS:治疗组为13.3个月,对照组为9.9个月;HR=0.52),患者疾病进展或死亡的风险降低了48%。
在另一项名为DYNAMO的2期临床试验中,研究人员还分析了duvelisib对惰性非霍奇金淋巴瘤的治疗效果。在这项研究中,接受治疗的患者对利妥昔单抗和化疗/放射免疫疗法产生了双重耐药性。在这些缺乏治疗选择的患者中,duvelisib达到了46%的客观缓解率(ORR),达到了主要临床终点。然而,在双重耐药滤泡性淋巴瘤患者亚组中,duvelisib的ORR也达到41%。
基于这两项临床试验的优异结果,Verastem向FDA提交了duvelisib的上市申请。
“Duvelisib上市申请的提交是Verastem的一个重要里程碑,也是我们员工和研究人员不断努力的结果。他们致力于为需要额外治疗的患者开发新的潜在治疗方案。我们也对过去几年中参与duvelisib临床试验项目的患者表示诚挚的感谢,”Verastem总裁兼首席执行官Robert Forrester先生说。“Duvelisib是第一个作为单一疗法的口服PI3K抑制剂,对复发性或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤患者有效。作为单药治疗,对双重耐药滤泡性淋巴瘤患者也显示出显著的临床疗效。我们相信duvelisib可以提供一个方便的口服治疗方案,我们期待在审查过程中与FDA合作,以便这种新药有望在2019年初获得批准。”
我们期待这种新药尽快问世,造福这些缺乏治疗的患者。
参考资料:
[1] Verastem向FDA提交了用于治疗复发或难治性慢性淋巴细胞性白血病/小淋巴细胞性淋巴瘤和滤泡性淋巴瘤的新药申请
[2]vera stem官方网站
关注药明康德微信官方账号
