自2020年新冠肺炎病毒爆发以来,全球疫情防控紧张,并呈反复上升趋势。尤其是奥米克隆的出现,加速了变异的传播,全球疫情依然看不到尽头。
疫苗作为对抗新冠肺炎最有力的武器,在中国、欧美等国家已经达到了很高的接种率,但在全球范围内,疫苗的分布仍然不平衡。例如,非洲的疫苗接种率仍徘徊在11%左右,远未达到世卫组织今年年中70%的目标。
为确保疫苗在全球范围内的公平公正分配,世卫组织早在2020年就与全球疫苗免疫联盟和防疫创新联盟共同制定了新冠肺炎疫苗实施计划(COVAX)。
世卫组织紧急使用清单(EUL)的授权是向包括COVAX机制参与国在内的许多国家出口疫苗的先决条件。
什么是EUL?
世界卫生组织官网介绍,EUL是世卫组织组建的一个机制,旨在评估新健康产品在突发公共卫生事件中的适用性,目标是尽快提供药物、疫苗和诊断工具。评估过程将严格审查疫苗第二阶段和第三阶段结束时的临床试验数据,以及大量关于安全性、有效性、质量和风险管理计划的附加数据。
在申请紧急使用清单的过程中,疫苗制造商必须承诺继续生成数据,直到疫苗获得世卫组织的完全许可和预认证。世卫组织预认证过程将在滚动的基础上评估疫苗试验和部署产生的更多临床数据,以确保疫苗符合必要的质量、安全和有效性标准,从而扩大疫苗供应。
查询世卫组织官网,新冠肺炎疫苗通过世卫组织审批需要三个阶段:
1.EOI接受:被世卫组织接受。
2.举行提交前会议:专家会议审查
3.接受审查的档案:临床试验病例审查
世卫组织下属的免疫战略咨询专家组(SAGE)负责审查证据,并就疫苗相关政策和剂量提出建议。
鉴于不同种类疫苗的功效、作用和效益难以进行简单的比较,涉及轻症、重症、重症需住院、储存要求、注射次数、常见和罕见副作用、费用等。因此,世卫组织评估疫苗的主要标准包括至少50%的有效率和生产制造标准。
对于疫苗R&D企业来说,进入应急使用名单意味着疫苗的安全性和有效性得到了认可。世卫组织批准的疫苗可以由联合国机构购买并分发给有需要的国家。未经世卫组织批准的疫苗只能由个别国家购买,而大多数国家没有购买力。
10种新冠疫苗获得WHO批准
根据世卫组织官网3月2日更新的世卫组织eul/pq评估过程中新冠肺炎疫苗的状况,目前,WHO已批准10种新冠肺炎疫苗紧急使用,分别来自辉瑞、阿斯利康、强生、Moderna、Novavax、Bharat Biotech、北药生物、中国生物制药等企业。
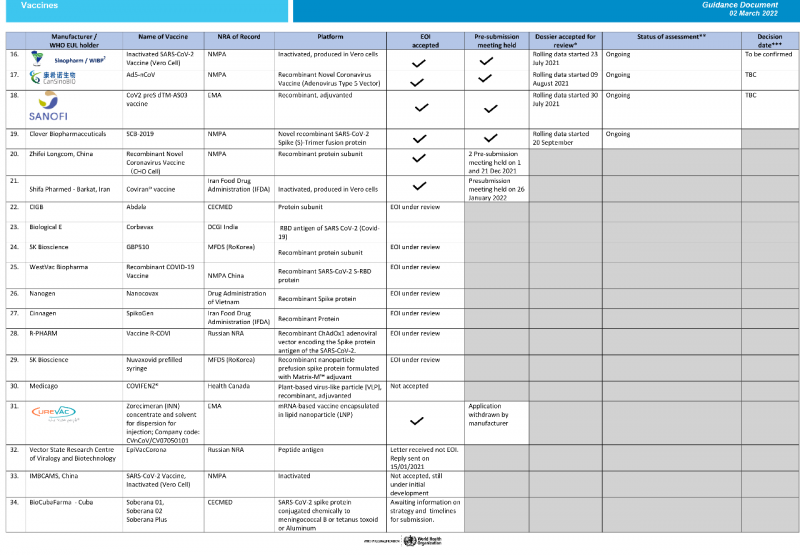
以下是截至2022年3月2日世卫组织疫苗在新冠肺炎获批的进展情况:
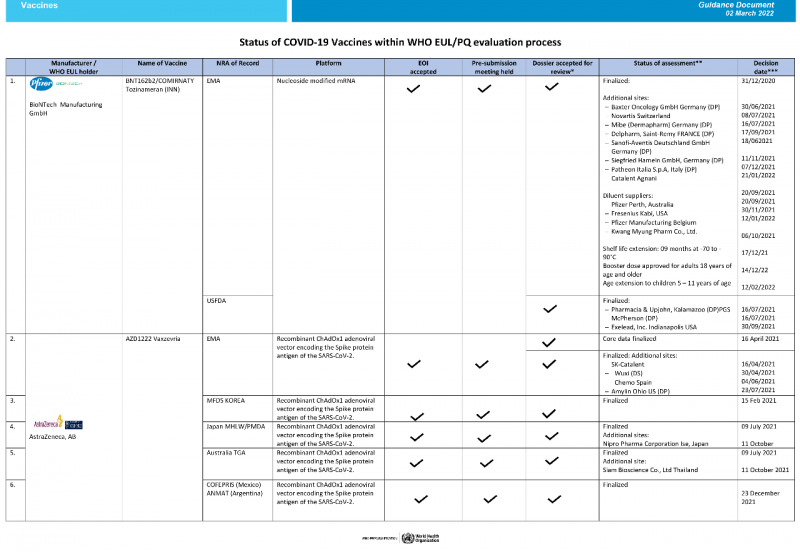

辉瑞/BioNTech的mRNA疫苗BNT162b2是世卫组织批准的第一种新冠肺炎疫苗。
2020年11月18日,辉瑞公布了BNT162b2的III期临床结果,该药物于12月2日在英国首次获准紧急使用。随后,它于12月11日和21日被美国美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准紧急使用,并于12月31日被世卫组织批准紧急使用。可谓进步神速。
为什么这么快就获批了?原因可能是辉瑞采用了“使用与EMA相关的简化程序”,即“使用欧洲药品管理局的便捷申请程序”。世卫组织有一个“严格监管机构”的名单,它相信在质量控制。当名单上的一个国家开发并批准一种疫苗时,世卫组织可以开启一个快速批准的便捷程序。不在名单上的国家需要世卫组织从头开始进行全面评估。这份名单包括美国、澳大利亚、加拿大、日本和一些欧洲国家。
随后,阿斯利康的腺病毒载体疫苗AZD1222、强生的重组蛋白疫苗、Moderna的mRNA疫苗mRNA-1273基于便捷的程序迅速获得世卫组织的批准。
此外,韩国SK生物公司和印度血清学研究所(SII)生产的阿斯利康疫苗Covishield也已获得世卫组织批准。
还有两个新冠肺炎的国产灭活疫苗,由EUL认证,分别来自中国生物-北京生物制品研究所(国药控股/BIBP)和北京科兴生物制品有限公司。
2021年5月7日,世卫组织批准将新冠肺炎疫苗纳入“紧急使用清单”,这是全球第六个被世卫组织纳入紧急使用清单的疫苗。这也是历史上第一次由非西方国家开发的传染病疫苗被世卫组织批准用于紧急情况。随后,6月1日,科兴生物的CoronaVac也获得了世卫组织的批准。
值得注意的是,虽然国药/WIBP的新冠肺炎疫苗早已在国内投入使用,但并未获得世卫组织批准紧急使用,相关评估仍在进行中。
此外,名单中还包括印度Bharat生物公司生产的灭活疫苗COVAXIN和Novavax公司的两种Matrix-M佐剂重组蛋白疫苗NVX-CoV2373/Nuvaxovid和NVX-CoV2373/CoVax。
6种国产新冠疫苗还在审评中
根据世卫组织3月2日更新的数据,除了已经批准的10种疫苗,还有20种疫苗正在接受世卫组织紧急使用清单(EUL)和资格预审(PQ)的评估。
其中6家来自中国,申请人为国药武汉生物、康希诺、志飞生物、三叶草生物、维克斯生物和医学科学院生物研究所。
其中,国药控股/WIBP的新冠肺炎灭活疫苗为新型冠状病毒灭活疫苗。
疫苗(Vero细胞)、新冠肺炎疫苗Ad5-nCoV(corn cino的腺病毒载体)、新冠肺炎疫苗SCB-2019(用作白三叶联合佐剂的三聚体重组蛋白)已完成验收和专家会议评审程序,正在进行三期临床试验病例评审。
新冠肺炎疫苗重组诺维尔冠状病毒疫苗(CHO细胞)仍处于世卫组织预认证和评估过程的第二阶段,其预申请已于2021年12月1日和21日提交。通过第二阶段后,再进行第三阶段的复习。
成都维氏生物的重组蛋白新冠肺炎疫苗和中国医学科学院医学生物学研究所生产的新型冠状病毒灭活疫苗(Vero细胞)尚未完成第一阶段审核。
参考来源: