它是世界上癌症相关死亡的第三大原因,最常见的类型是肝细胞癌(HCC)。手术切除是早期肝细胞癌的标准治疗方法。然而,多达70%的患者在手术后仍然会复发,并且没有围手术期干预显示存活益处。
最近,《柳叶刀-胃肠病学和肝脏病学》最近发表了西奈山伊坎医学院团队的2期临床试验结果。研究表明,近1/3患者术前新辅助免疫治疗(PD-1抑制剂)诱导肿瘤细胞大面积死亡(50%)。
论文指出,这是“迄今为止报道的最大规模的肝癌PD-1抑制剂单药新辅助治疗临床试验。”研究中观察到的病理缓解支持更大规模试验的设计,以进一步确定最佳治疗持续时间并阐明临床益处。

截图来源:柳叶刀胃肠病学肝病
以往的研究初步表明,新辅助免疫治疗可以诱导各种肿瘤类型的病理缓解,并可能降低肝癌术后复发的风险。新的辅助免疫疗法不仅可以杀死肿瘤,还可以通过持久的免疫反应杀死手术无法完全消灭的微小癌细胞,而这些微小癌细胞可能会导致未来的癌症复发或转移。因此,本研究的目的是评估可切除肝细胞癌患者中塞米单抗新辅助治疗的临床活性。
这是一项单组、开放性的2期试验。共纳入21名可切除肝细胞癌(Ib、II和IIIb期)患者。患者接受了新辅助治疗Cemlimab (350 mg静脉输注,每3周治疗两个周期),然后进行手术切除,然后辅助治疗Cemlimab (350 mg静脉注射,每3周治疗8个周期)。
研究的主要终点是通过病理学检查发现显著的肿瘤坏死(定义为切除肿瘤的70%坏死)。次要终点包括手术延迟、总体缓解率、CD8 T细胞密度变化和不良事件。分析所有接受至少一剂塞米单抗并完成手术切除的患者的肿瘤坏死和缓解率;在意向性治疗人群中分析安全性和其他终点。患者在治疗前进行了活检,并在整个治疗过程中进行了采血。
所有患者均接受了新的辅助治疗,其中20例患者成功切除肿瘤。其中4例(20%)新辅助免疫治疗后出现明显肿瘤坏死,其中3例(15%)完全坏死。7例(35%)患者肿瘤坏死率50%。根据影像学结果,3例(15%)患者达到部分缓解(肿瘤体积缩小30%),其他患者疾病均保持稳定。
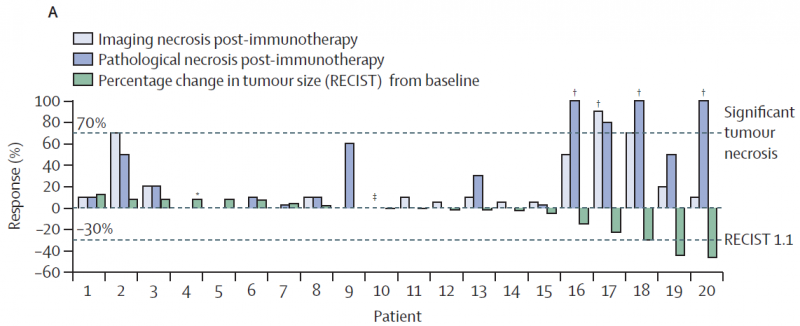
20例手术患者的缓解(影像学)和肿瘤坏死(影像学和病理学)。(图片来源:参考文献[1])
肿瘤坏死的MRI评价结果与病理评价结果密切相关,但坏死的评价结果(无论是病理还是影像)与肿瘤缓解结果仅中度相关,且这种相关性不显著。这种差异表明,每个指标在量化肿瘤体积缩小方面都有其自身的局限性。
免疫组化分析显示,坏死率50%的患者治疗前往往免疫细胞较多,治疗后免疫浸润密度和肿瘤浸润淋巴细胞进一步增加,其中CD8 T细胞浸润明显增加。换句话说,在治疗前免疫系统已经在与癌症作斗争的患者往往对免疫疗法有更多的反应,他们的免疫系统将被免疫疗法进一步激活。
治疗安全性是可以接受的。没有患者因为不良事件而取消手术。新辅助免疫疗法的一个可预见的潜在障碍是由于毒性风险而导致的根治性手术的延迟。在这次试验中,只有一名患者出现肺炎,导致手术推迟了2周。
20名患者(95%)在新辅助治疗期间出现任何程度的治疗相关不良事件。任何级别中最常见的不良事件是天冬氨酸转氨酶升高(4例)、肌酸磷酸激酶升高(3例)、便秘(3例)和疲劳(3例)。
7例患者出现3级不良事件,包括血清肌酸磷酸激酶升高(2例)和低白蛋白血症(1例)。
没有观察到4级或5级事件。
“我们认为患者术前接受免疫治疗更好,因为人在转移前更健康,免疫系统处于更好的状态,可以更好地抵抗癌症。结合许多其他类型肿瘤的新辅助免疫治疗试验的结果,这项研究支持了评估围手术期免疫治疗策略以降低复发风险的必要性。”该研究的作者,西奈山伊坎医学院的托马斯马龙教授说,“未来,更大规模的试验将有助于确定新的辅助免疫疗法的实用性,安全性和生存效益。”
同期的综述文章也指出,未来的研究应考虑最合适的药物组合、最佳治疗持续时间以及基于危险因素的后续术后治疗。早期疾病活动指标(如肿瘤坏死)与复发风险持续降低之间的相关性仍有待证实。