2017年8月18日,美国总统签署了"食品药物管理局重新授权法”(FDARA),其中通过重新授权的还包括截止到2022年9月的《仿制药用户收费案》 (GDUFA)。
今天,美国食品和药物管理局微博发文称"这是美国公共卫生事业的一个胜利"。
非专利药品使用者收费重新授权:公共卫生的胜利
作者:凯瑟琳乌尔,迈克尔科普沙,
我们在2017年10月一日标志着仿制药计划中的一个重要里程碑——仿制药使用者费用修正案(GDUFA)第一次重新授权的开始。这些来自行业的费用为食品及药物管理局提供了重要的资金,推动了该机构审查和批准仿制药申请的监管工作。

凯瑟琳乌尔,岁,是食品及药物管理局药物评估和研究中心仿制药办公室主任
这不仅是食品及药物管理局的里程碑,也是公共卫生的胜利。增加消费者获得安全、高质量和可负担得起的仿制药是食品及药物管理局的首要任务。学名药的价格通常只是名牌药的一小部分,几乎十分之九的处方都是用学名药开的。在过去十年中,仿制药为美国医疗保健系统节省了近1.7万亿美元。
虽然食品及药物管理局在确定药物定价方面没有直接作用,但当一种药物的多个仿制药版本获得批准时,它会刺激竞争,并为消费者提供负担得起的选择。
国会于2012年首次批准向行业收取使用费,以帮助资助食品及药物管理局的仿制药项目,为期五年。除了传统的国会预算拨款之外,在更长的一段时间内获得另一个资金来源,使我们能够雇用更多的工作人员,更好地分配我们的审查活动。因此,美国食品和药物管理局批准了创纪录数量的仿制药申请。
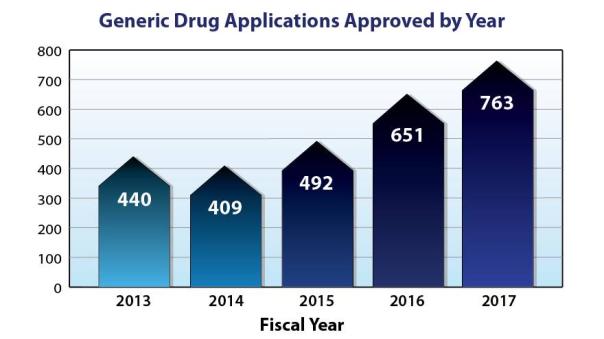
事实上,目前批准的所有仿制药的25%是在修正案的第一个五年期间批准的。在修正案的最后两年,美国食品和药物管理局每年批准的仿制药比仿制药项目历史上任何一年都多100 . gdu fa的重新授权将有助于我们在这一成功的基础上再接再厉。

迈克尔科普沙是美国食品和药物管理局药物评估和研究中心药物质量办公室主任
使用者付费支持专门的食品及药物管理局工作人员审查仿制药申请和检查生产仿制药的设施。用户付费为重要的信息技术基础设施提供资金,帮助食品及药物管理局管理不断增加的工作量、提高效率并增加透明度。他们还资助重要的监管研究,这些研究有助于澄清和改善作为仿制药产品评估基础的科学和临床理解。
我们在修正案重新授权中同意的目标和承诺支持公共卫生。我们现在对公共卫生优先领域的申请有了更短的审查目标。此外,这些目标促进了两个主要目标:减少批准仿制药申请的时间和增加批准的仿制药数量。我们加强了与行业的沟通,以帮助确保该机构收到完整、高质量和科学合理的申请。另一个新功能是灵活的用户收费结构,以满足小型企业的需求。这鼓励了竞争,反过来可以降低消费者的药价。
开发复杂药物产品的仿制药——如吸入药物或某些类型的注射药物——具有独特的挑战100 .林业局将更早、更频繁地会见申请人,以预测这些产品开发中可能出现的挑战。
我们在修正案的经验使我们能够改进审查流程,并实施与行业和消费者沟通的最佳实践100 . gdu fa的重新授权建立在头五年的成功基础上。我们期待在未来五年帮助美国公众获得更多负担得起的高质量仿制药。
请访问/仿制药了解更多关于食品及药物管理局仿制药计划的信息,并跟踪重新授权的修正案的进展情况。
凯瑟琳乌尔,岁,是食品及药物管理局药物评估和研究中心仿制药办公室主任
迈克尔科普沙是美国食品和药物管理局药物评估和研究中心药物质量办公室主任
来自:FDA之声
原标题:美国总统重新授权《仿制药用户收费案》 ,美国公共卫生事业的一个胜利