癌症免疫治疗是改变癌症治疗模式的革命性突破。然而,即使几种FDA批准的免疫疗法已经上市,也只有少数癌症患者能够从中受益。这是因为癌细胞也非常狡猾,它们可以使用各种手段来防止被免疫细胞靶向和破坏。目前,各种免疫检查点抑制剂的作用靶点是癌细胞逃避免疫系统“追捕”的手段之一。研究人员也在努力更加全面系统地了解癌细胞免疫逃逸的机制。
日前,来自多伦多大学和Agios Pharmaceuticals的研究人员合作,利用CRISPR筛选技术系统地搜索了导致癌细胞逃脱免疫系统攻击的驱动基因。他们发现很多与自噬相关的基因是免疫逃逸的关键!这项研究发表在顶级科学杂志《自然》上。

CRISPR敲除筛选发现182个“核心免疫逃逸基因”
为了系统地研究不同基因对癌细胞逃脱免疫系统攻击的影响,研究人员使用CRISPR-Cas9技术构建了一个能够敲除19069个编码蛋白质的基因的指导RNA(gRNA)库。使用这种工具,他们逐个敲除了六种不同癌细胞系中编码蛋白质的基因。这六种癌细胞系来源于乳腺癌、结肠癌、肾癌和皮肤癌,代表了具有非常广泛遗传背景的癌症模型。
研究人员将这些细胞系与活化的细胞毒性T细胞(CTL)放在一起,观察哪些基因在敲除后使癌细胞对CTL更敏感,哪些基因在敲除后使癌细胞抵抗CTL攻击。筛查的结果发现了182个基因,这些基因在3种以上的细胞系中表现出相同的能力,能够让癌细胞对CTL的杀伤作用更为敏感或更具有抗性。研究人员称这些基因为“核心癌症固有免疫逃逸基因”(core cancer intrinsic immune evasion genes)。
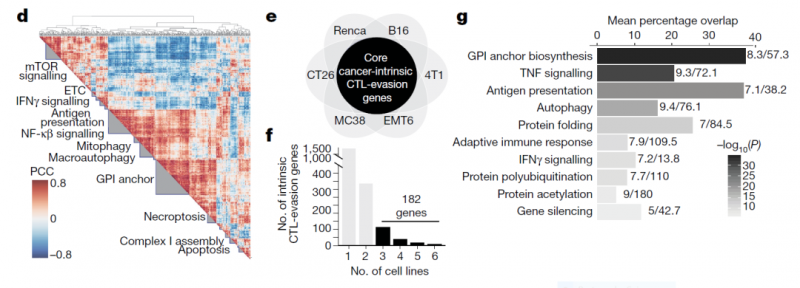
通过CRISPR敲除筛选6种不同的癌细胞系,发现了182个基因(图片来源:参考文献[3])
自噬信号通路在免疫逃逸中的关键作用
通过分析这182个基因的特征,研究人员发现其中许多基因与调节干扰素(IFN)的信号通路有关。干扰素-是一种细胞因子,在许多免疫反应中起重要作用。进一步分析表明,许多与自噬相关的基因在调节干扰素-的信号通路中起着关键作用,其中一些基因以前没有发现与干扰素-相关。例如,研究人员发现了一种叫做FITM2的基因,它在小鼠脂肪组织的脂肪储存中起着关键作用。然而,如果FITM2基因在细胞中被敲除,它会使三种癌细胞株对CTL更敏感。
阐明自噬的研究获得了2016年诺贝尔生理学或医学奖。自噬作用好像细胞内的“废物回收站”,通过回收自噬过程中产生的氨基酸,细胞可以为合成新蛋白和构建细胞器提供原料。在之前的研究中,研究人员发现,抑制自噬的药物与其他抗癌药物联合使用,可能会产生更好的抗癌效果。例如,几个研究小组发现,自噬抑制剂与MAPK信号通路抑制剂结合可以抑制不同类型肿瘤的生长。
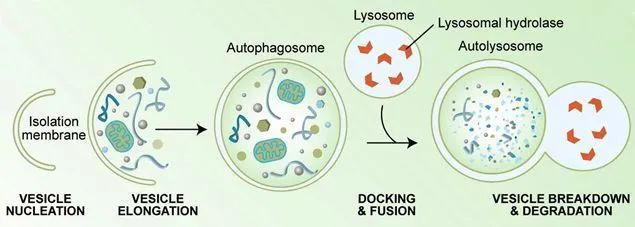
自噬过程示意图(来源:参考文献[4])
在这项研究中,研究人员发现,一种名叫autophinib的自噬抑制剂可以使许多肿瘤细胞系对另一种细胞因子TNF更加敏感,TNF在细胞免疫反应中起着重要作用。这表明抑制自噬可能具有提高免疫治疗效果的潜力。
“负负得正”的意外发现
同时,研究人员在论文中指出,不同基因之间的相互作用可以对肿瘤细胞的免疫逃逸产生很大影响。当他们研究与自噬相关的基因之间的相互作用时,发现敲除带有ATG12名称的基因会使肿瘤细胞对细胞毒性淋巴细胞更加敏感。然而,同时敲除ATG5或ATG16L1会使肿瘤细胞对细胞毒性淋巴细胞产生耐药性。这一结果表明,肿瘤已经携带的一些基因突变可能决定了特定靶向药物能否抑制癌症进展或“适得其反”。
最后,在论文的讨论中,研究人员表示,这项研究中发现的介导肿瘤从细胞毒性T细胞中逃逸的核心基因和信号通路,可能为指导新的癌症免疫疗法的开发提供了见解。
参考资料:
[1]科学家发现了几十种让癌细胞逃避免疫系统的基因。检索于2020年9月24日,来自
[2] Agios有助于识别让癌症逃避免疫系统的基因。检索于2020年9月24日,来自
[3]劳森等人,(2020年)。癌症的功能基因组景观相当于-ED细胞对杀伤的内在逃避。自然,
[4]虫书:在线评论秀丽隐杆线虫生物学。2019年5月9日检索,来自
关注【药明康德】微信公众号
