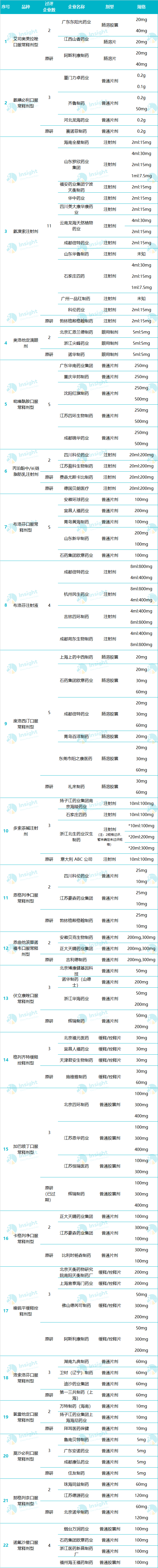
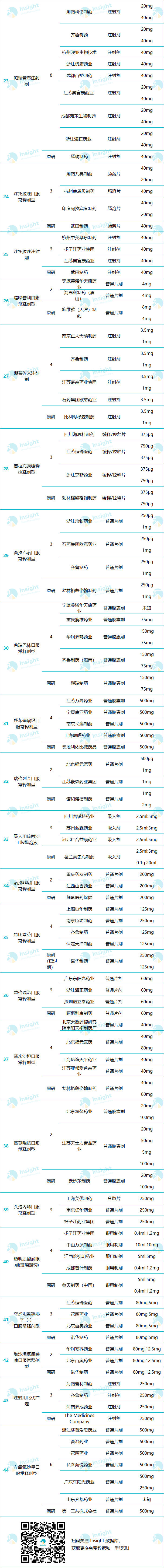
1月5日,NMPA发布最新批文,又有15个仿制药获批,17个仿制药通过一致性评价。其中,
1个仿制药首次接受评估,包括7次注射;
第四批国家品种已有8个通过企业评审,竞争形势日趋激烈;
傅和齐鲁都迎来了三个新评产品,齐鲁获得了一个新的首仿;
注射用奥美拉唑钠,60亿级PPI,江苏奥赛康首次评估。
今天评估/批准的品种详情如下:
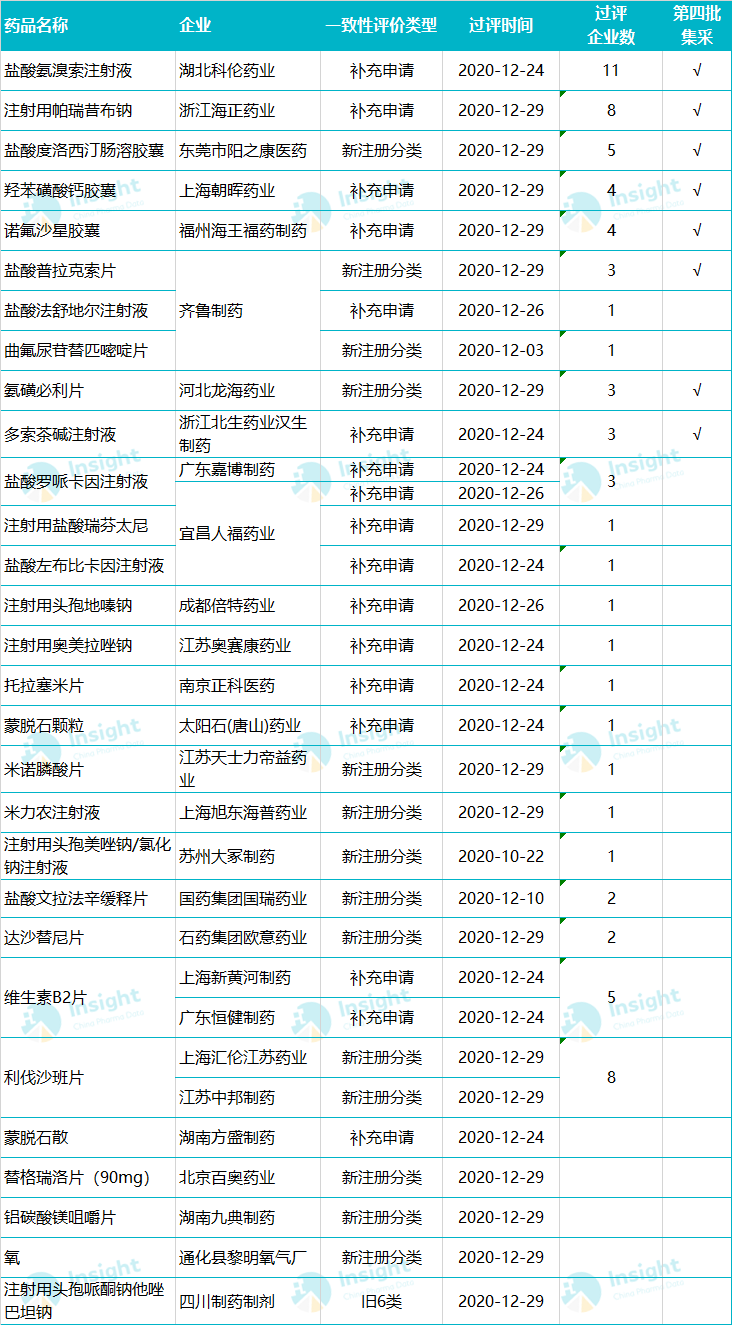
60 亿级重磅品种「注射用奥美拉唑钠」,
奥赛康首家过评
奥美拉唑是质子泵抑制剂的代表药物。注射用奥美拉唑钠能抑制H-K-ATP ATP酶,是临床上主流的抗胃酸药物。主要用于消化性溃疡及其出血,临床治疗效果好,不良反应少。
公开数据显示,目前已上市的PPI药品大部分市场规模超过10亿,其中注射用奥美拉唑钠最好,其2019年国内公立医疗机构终端销售额达63.9亿元。另一个重量级PPI——注射用泮托拉唑钠2019年销售额也达到67.1亿元。但从2020年11月开始,PPI药物开始逐步评估。
根据Insight数据库,除了原阿斯利康,目前注射用奥美拉唑钠是第一个接受评估的。此外,20家企业提交了一致性评价补充申请,竞争激烈;79家企业无进展。
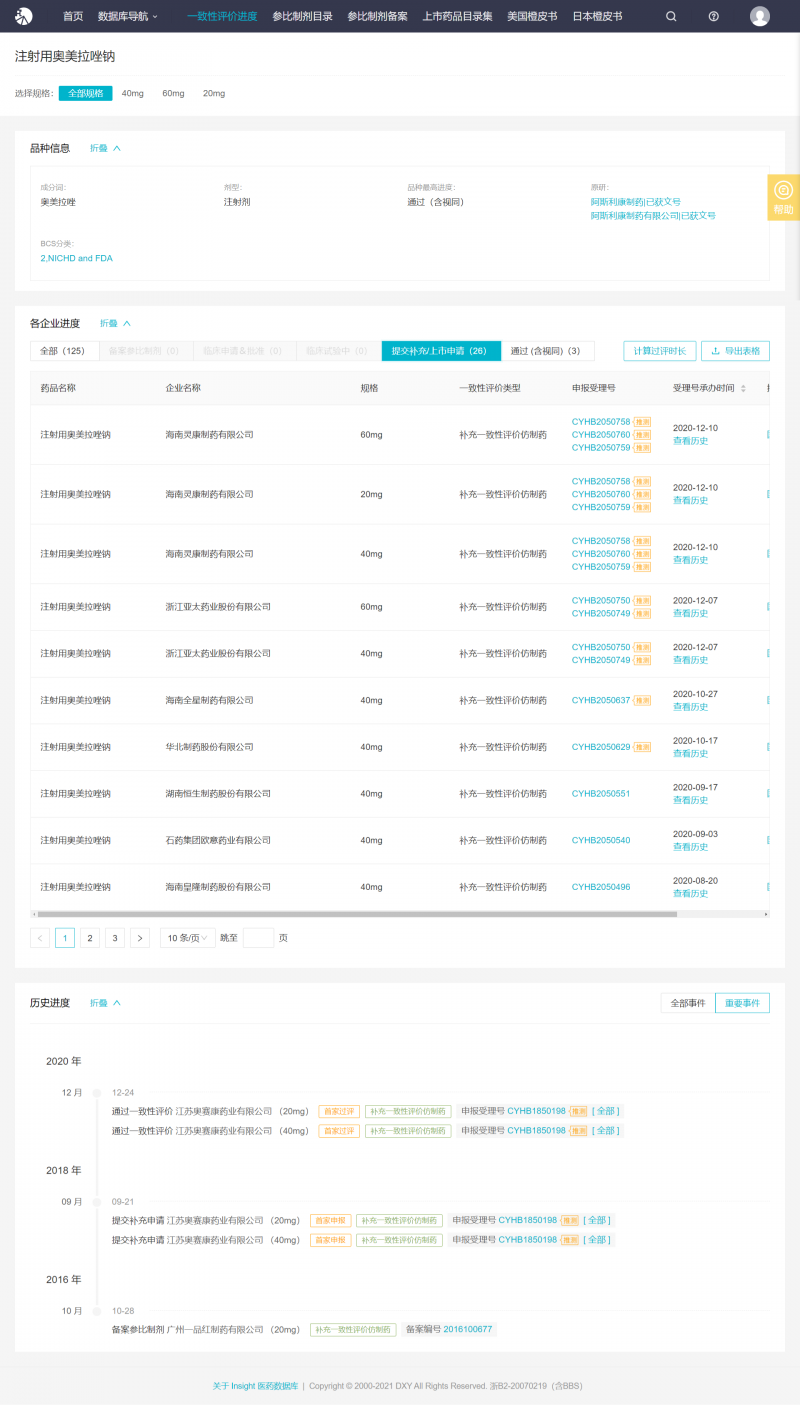
来自Insight数据库()
江苏奥赛康是该品种中第一家提交一致性评价补充申请的企业,2018年9月开始申请。此外,值得一提的是,乐施会也是另一个重量级PPI——注射用泮托拉唑钠首个被高估的企业。
齐鲁制药收获 1 款首仿,1 款首家过评
NMPA官网显示,齐鲁制药有限公司的‘盐酸普拉沙林片’和‘三氟尿苷替比脒片’按照新的注册分类获得批准,盐酸法舒地尔注射液已通过一致性评价。其中,三氟尿苷替比脒片为国内首仿,法舒地尔注射液为首评,普拉沙林属于第四批国家品种。
Insight数据库显示,除齐鲁制药外,已有5家公司提交盐酸法舒地尔注射液补充申请,1家公司提交新的注册上市申请,31家公司无进展。
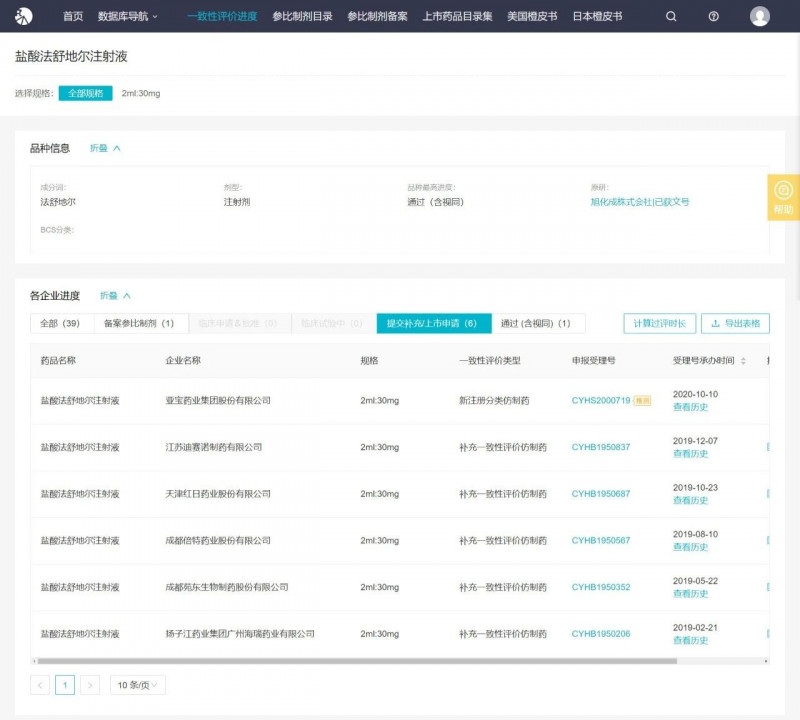
来自Insight数据库()
目前国内批准的只有最初在日本研发的大鹏,齐鲁制药被批准为国内首仿。除了齐鲁制药股份有限公司,只有郑达天晴公司提交了新注册和分类上市申请。
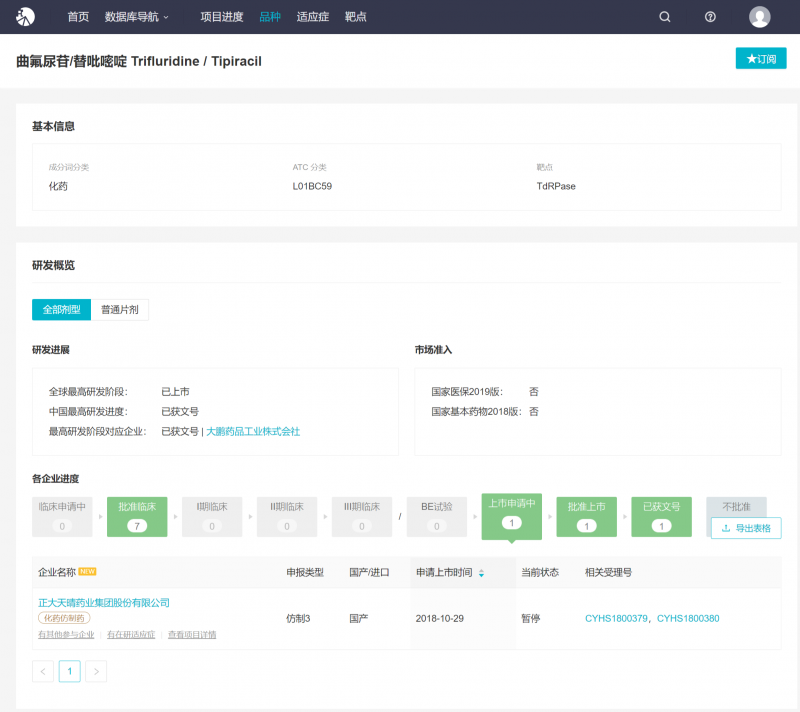
来自Insight数据库()
盐酸普拉克索片是第四批国家品种。本次齐鲁评估后,有四家公司参与竞争:齐鲁制药、京信制药、优诺康和颜渊勃林格殷格翰,另有两家公司提交了新的注册和分类上市申请。
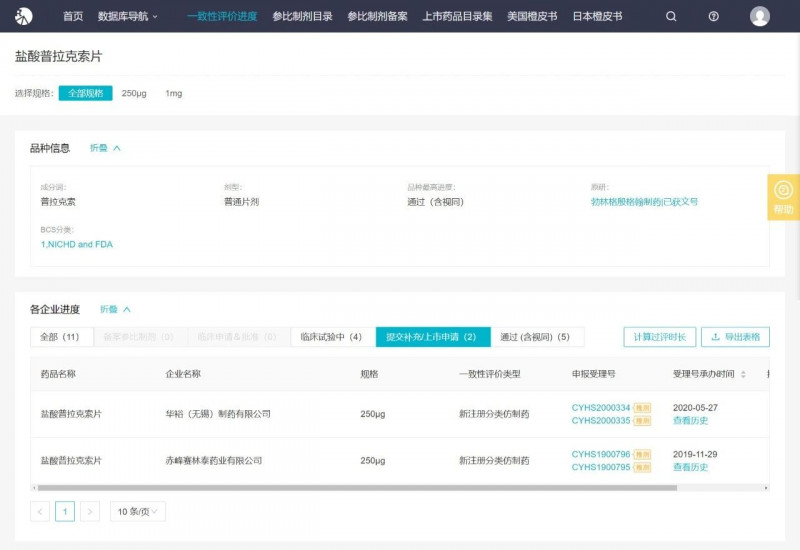
附:
第四批采用国家最新产品规范的企业详情
(截至2021年1月5日)