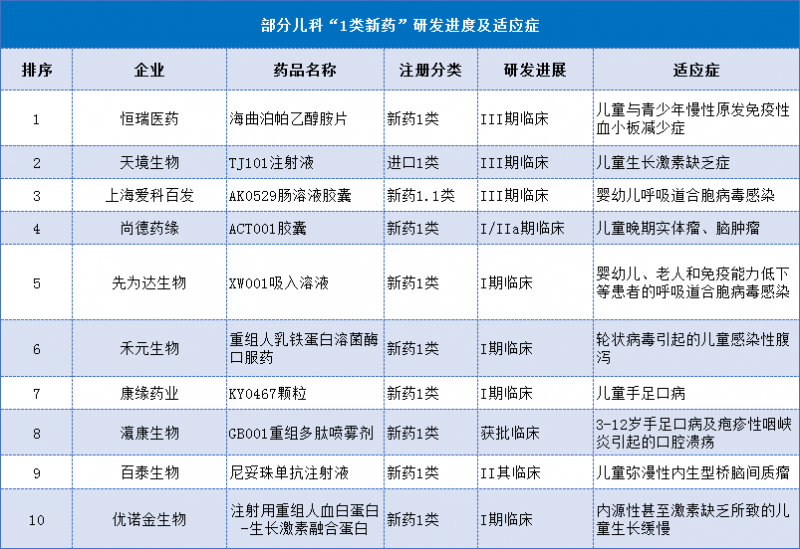
2022年5月11日,上海市药品监督管理局官网发布公开征求意见通知《上海市自体CAR-T细胞治疗药品监督管理暂行规定》。公开征求意见时间为2022年5月11日至6月10日。本次《上海市自体CAR-T细胞治疗药品监督管理暂行规定》规定了自体CAR-T细胞治疗药物的监督管理要求,弥补了我国自体CAR-T细胞药物监督管理要求领域的空白。
1、CAR-T细胞治疗产品
是“医学”还是“医疗技术”?
CAR-T细胞,即嵌合抗原受体T细胞,是通过基因修饰技术,将具有特异性抗原识别结构域和T细胞激活信号的遗传物质转入T细胞中,使T细胞直接与肿瘤细胞表面的特异性抗原结合而被激活,通过释放穿孔素、颗粒酶B等直接杀伤肿瘤细胞的T细胞。同时招募人体内源性免疫细胞,通过释放细胞因子杀死肿瘤细胞。
根据当时卫生部《上海市自体CAR-T细胞治疗药品监督管理暂行规定》等相关规定和要求,自体干细胞和免疫细胞治疗被列为第三类医疗技术进行管理。鉴于细胞治疗技术的逐步完善,2017年12月,中国食品药品监督管理局药品审评中心发布了《医疗技术临床应用管理办法》(试行),代表了细胞治疗产品由“三类医疗技术”向“药品”监管的转变。本指导原则明确了细胞治疗产品是指来源于人类的活细胞产品,用于治疗人类疾病,来源、操作和临床试验过程符合伦理要求,并根据药品管理相关法律法规进行研发和注册。
2、自体CAR-T细胞药品商业化
挑战与对策。
1.细胞治疗产品人员有哪些特殊考虑?
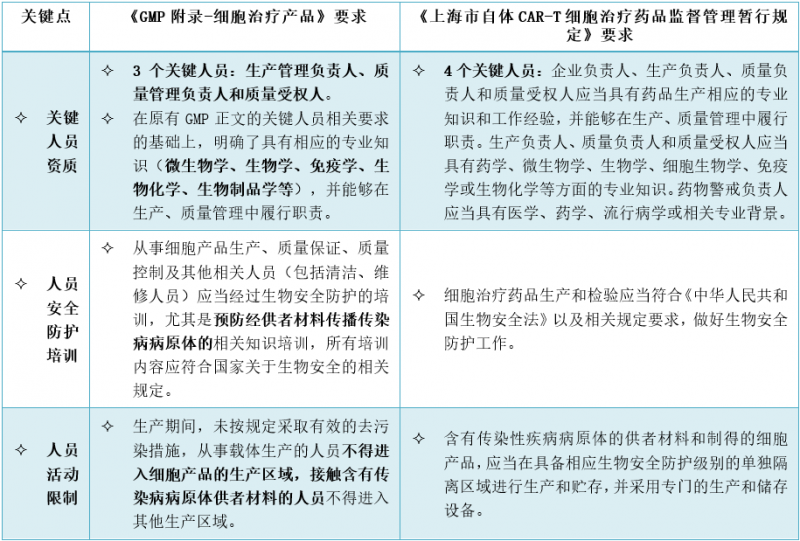
2.细胞治疗产品的生产设施和设备有哪些特殊的考虑?
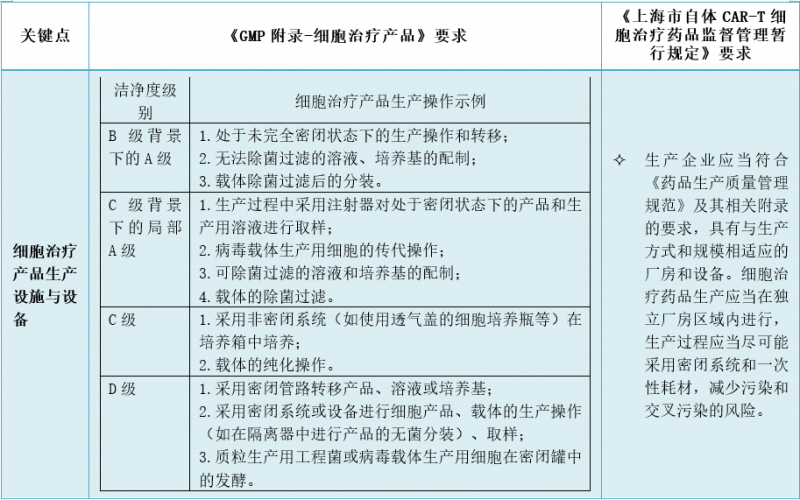
3.细胞治疗产品的材料有哪些特殊的考虑?

4.细胞治疗产品的生产管理有哪些特殊的考虑?
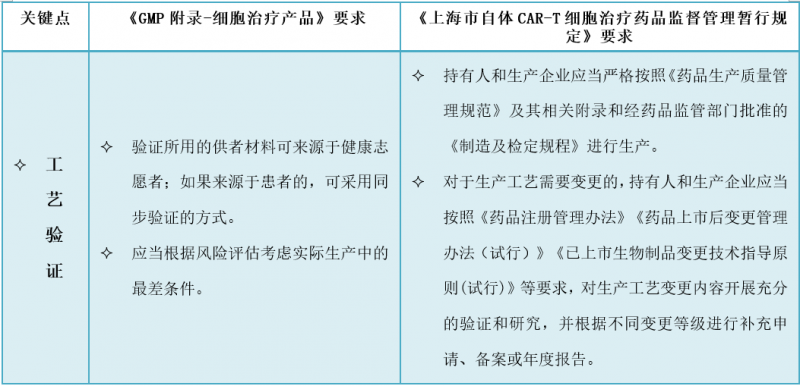
5.细胞治疗产品的质量管理有哪些特殊考虑?

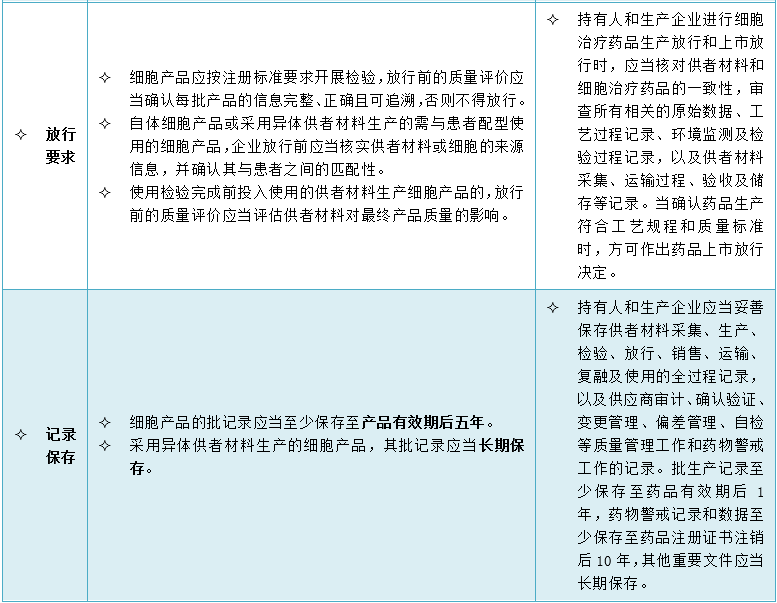
6.产品追溯系统有哪些特殊考虑?
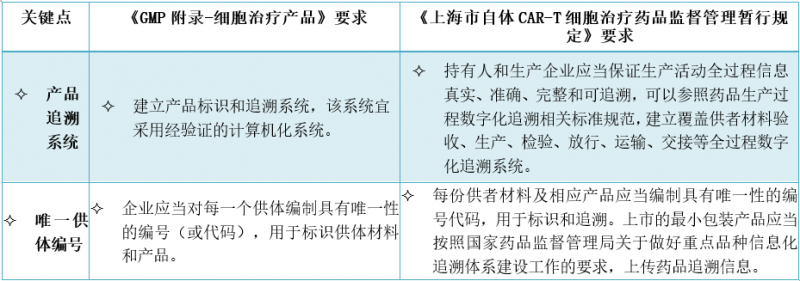
3、小结
细胞治疗产品是新药研发的热点。细胞治疗产品的商业化生产对医疗机构和患者来说面临着诸多风险,甚至影响到细胞治疗产业的健康发展。作为国家科技中心和生物医药研发产业的重要场所,上海在细胞治疗产品的研发方面相当活跃,并已开始走产业化的基础。
为解决细胞治疗商业化的瓶颈,上海美国食品药品监督管理局起草了《细胞治疗产品研究与评价技术指导原则》,将加快细胞治疗的商业化和标准化进程,为我国细胞治疗行业监管标准的制定提供有益参考。
参考资料来源:[1]上海市药品监督管理局