摘要:
三月份,CDE处理了622份药品注册申请。
三家公司提交了非专利吲达帕胺片一致性评价的申请。
和记黄埔宣布呋喹替尼胶囊的新适应症
齐鲁制药富马酸苯丙酚替诺福韦片完成上市申请。
Xi安让桑前列腺癌新药阿帕鲁胺片申请国内上市。
7个品种第一家企业通过一致性评价。
总体承办情况
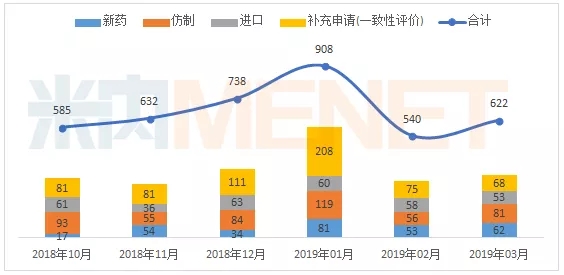
据MED中国药品审评数据库2.0统计,2019年3月,CDE共受理药品注册申请622件,总体呈上升趋势。新药申请和仿制申请均较上月增长,进口申请基本持平,补充申请(一致性评价)继续回落。
2018年10月至2019年3月承担的药品注册申请(按受理号)
一致性评价承办情况
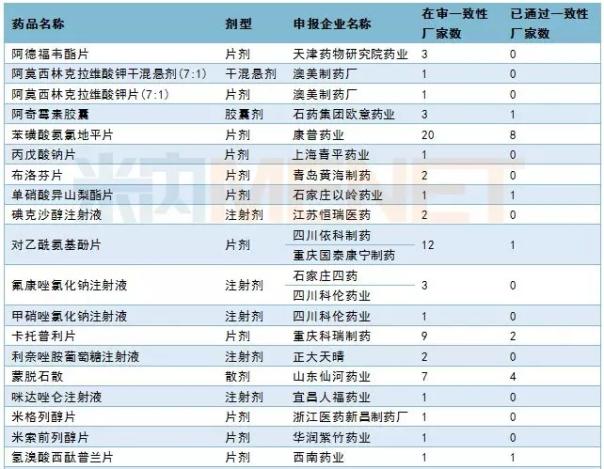
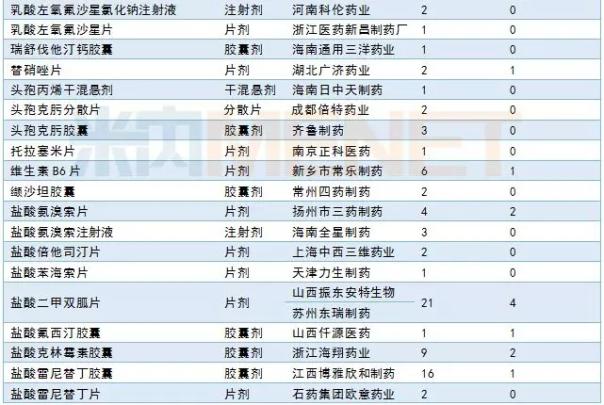
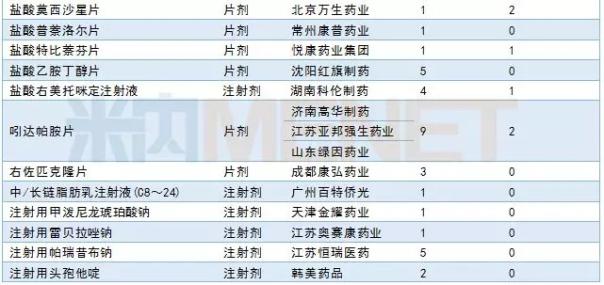
3月,CDE承担了50个一致性评价品种,包括13个注射剂。三家公司提交了吲达帕胺片一致性评价申请:济南高华制药、江苏亚邦盛强制药和山东路引制药。有关详细信息,请参见下表:
2019年3月CDE补充申请(一致性评价)品种承诺书
国内新药申请承办情况:和记黄埔申报呋喹替尼新适应症
3月份,CDE签约了31种新药,其中24种属于一类新药。和记制药宣布呋喃西林胶囊的新适应症。杭州中美华东制药GLP-1激动剂TTP273申报临床。有关其他信息,请参见下表:
2019年3月国内新药申报承诺书
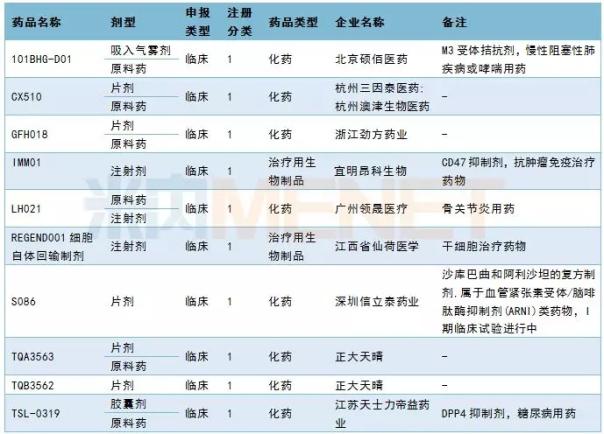
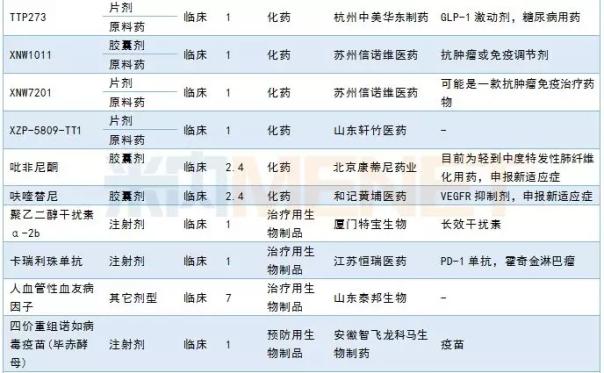
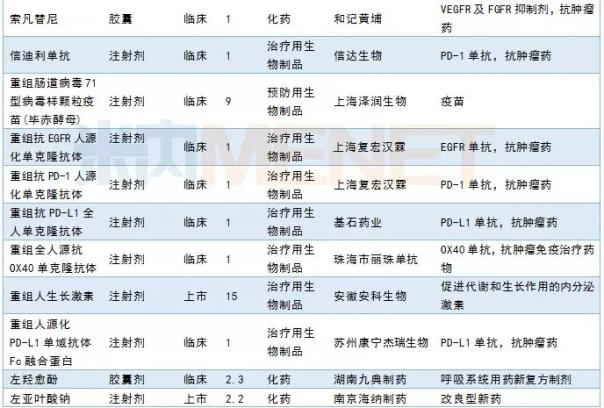
国内仿制申请承办情况:齐鲁制药TAF完成BE申请上市
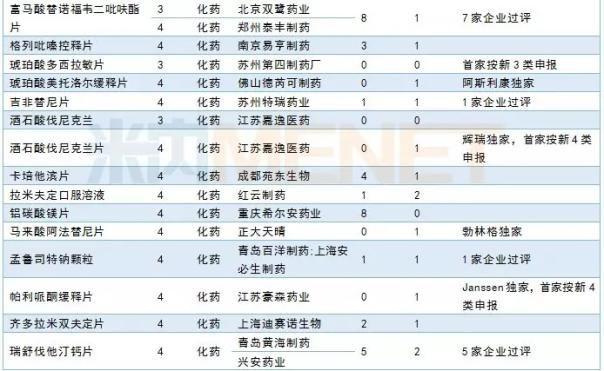
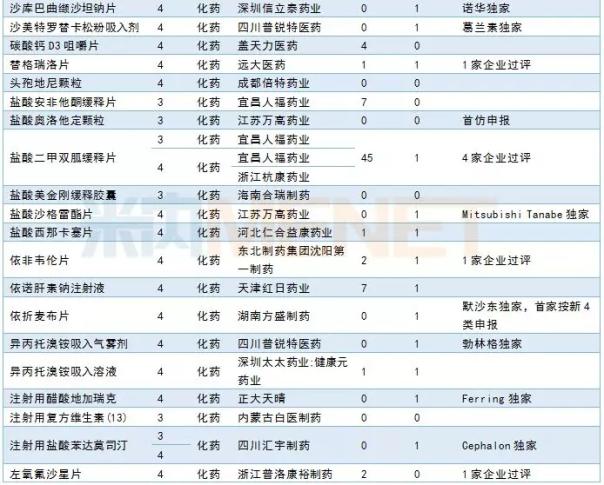
3月份,CDE共受理了50个品种的仿制申请。其中14个品种为目前国内独家品种,12个品种通过了企业一致性评价。齐鲁制药有限公司的TAF完成了BE提交的仿制申请,江苏王奥制药有限公司率先提交了盐酸奥洛他定颗粒的仿制申请。有关其他信息,请参见下表:
2019年3月国内仿制申请承接情况
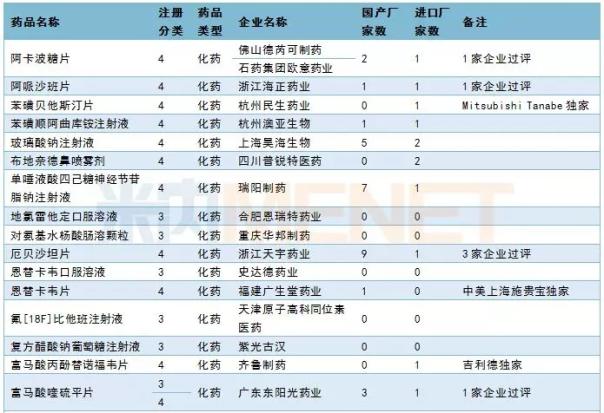
进口申请承办情况:西安杨森阿帕鲁胺申请上市
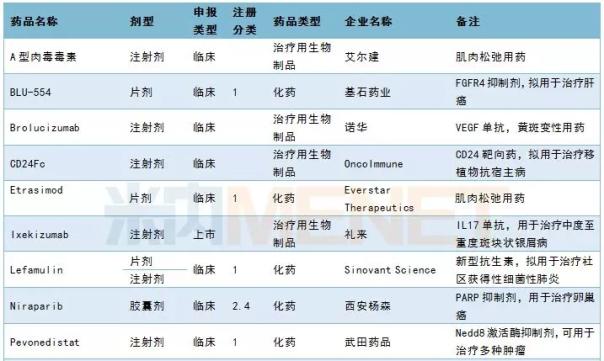
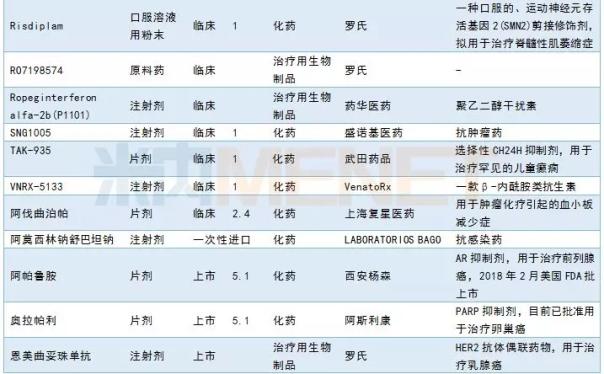
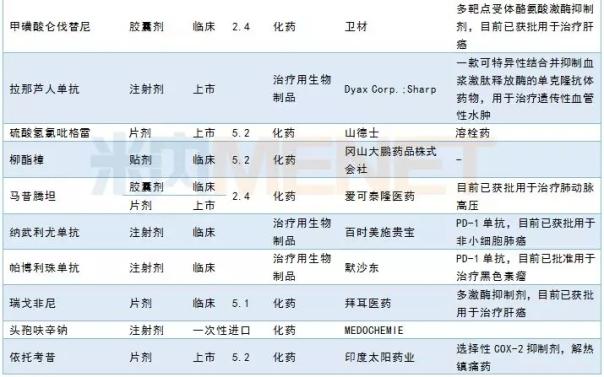
3月份,CDE共处理了30个药品进口申请,包括8个第1类新药和3个第5.2类进口仿制药。Xi安让桑提交了前列腺癌新药Aparu amine的上市申请。
2019年3月进口申请承诺
获批情况:7个品种首家企业过评
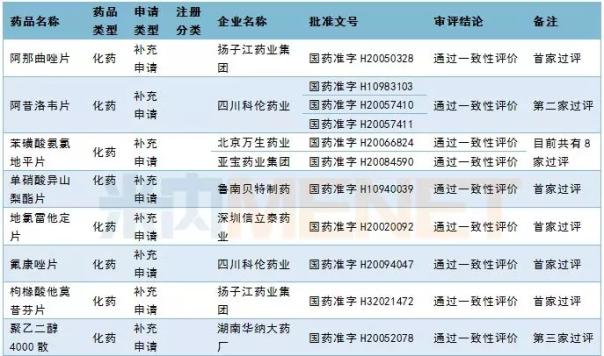
3月,12个品种(20个规格)通过仿制药一致性评价,其中7个品种为首批通过评价的企业。根据我国公立医疗机构终端竞争格局,2017年阿那曲唑片、单硝酸异山梨酯片、替莫唑胺胶囊销售额均超过10亿元。江苏豪森制药公司和齐鲁制药公司的维格列汀片仿制药申请均于3月获批。
2019年3月批准部分品种
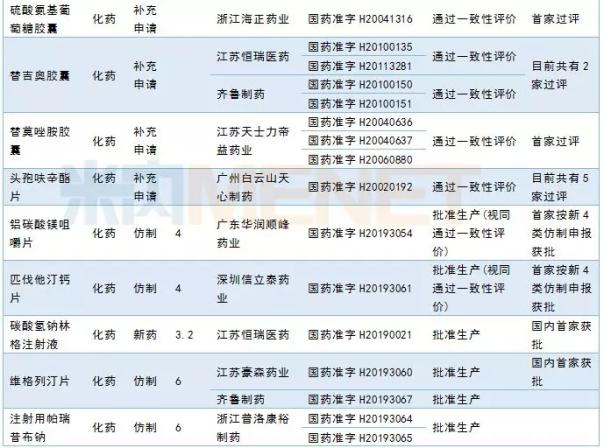
统计截至2019年4月2日,按品种名称。