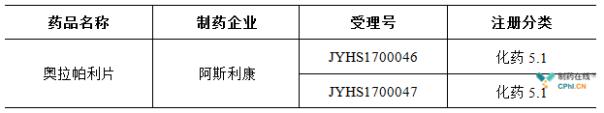
最近,阿斯利康拥有的药物Orapali片剂在中国上市的申请已经过审查,预计将获得批准上市。这种药物将很快成为第一个在中国批准上市的PARP抑制剂。
阿斯利康奥拉帕里片的国内进口和上市申请于2017年12月由CDE接受并承担。2018年1月,以‘与现有治疗方法相比具有明显治疗优势’为由,将其列入第26批CDE药品注册申请纳入优先审评程序。快速审评的完成得益于国内加快临床急需新药审批的政策。
2017年,PARP抑制剂全球销售额总计4.62亿美元,其中奥拉帕尼贡献了2.97亿美元。作为治疗卵巢癌患者的重磅药物,奥拉帕里片的上市将填补我国卵巢癌靶向治疗领域近30年的空白,惠及我国广大卵巢癌患者。
全球首款PARP抑制剂
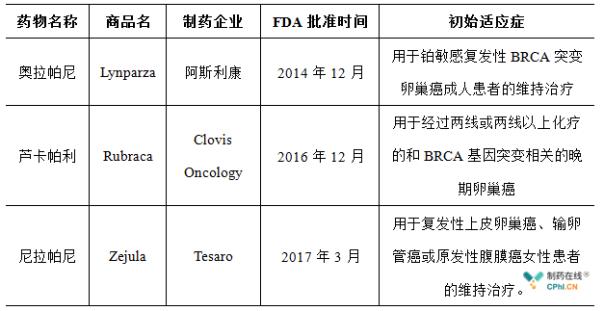
奥拉帕利胶囊于2014年12月获得FDA批准上市。它是世界上第一个PARP抑制剂,其最初批准的适应症是用于治疗铂敏感的复发性卵巢癌。自上市以来,阿斯利康一直在积极开发奥拉帕尼的多种适应症,并先后被批准用于卵巢癌、输卵管癌、原发性腹膜癌和乳腺癌。此外,包括由BRCA突变引起的胃癌在内的许多适应症正处于临床阶段。
到目前为止,全球批准的PARP抑制剂有三种。继阿斯利康的Orapali之后,Clovis Oncology的Lucapali是第二个获准上市的PARP抑制剂。该药可作为治疗BRCA基因突变相关的晚期卵巢癌的单一疗法;这两种药物的一个共同点是,患者在使用药物前需要提前进行BRCA基因突变检测。尼拉帕尼,第三个批准上市的PARP抑制剂,是FDA批准的第一个PARP抑制剂,可以直接用于治疗。患者在使用时不需要提前检测BRCA突变或其他生物标志物。根据CFDA官方网站,截至本文发表之日,卢卡帕格利和尼拉帕尼尚未提交在中国注册和上市的申请。
本土PARP抑制剂开发战况概览
PARP抑制剂作为抗肿瘤药物研发的热点靶点之一,是卵巢癌治疗最有前景的靶向药物,国内多家药企都在针对该靶点研发药物。据不完全统计,目前国内有8家本土药企的PARP抑制剂产品正在研发并获批临床应用,包括百济神州、再鼎医药、江苏豪森、庆丰医药、人福医药、恒瑞医药、上海创诺医药、中科院上海药物所。
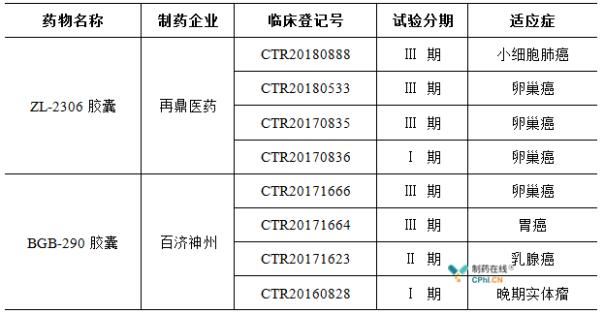
其中,国内处于三期临床试验阶段的药物有百济神州的BGB-290胶囊和再鼎医药的ZL-2306胶囊,两者均涵盖卵巢癌。此外,再鼎医药的ZL-2306胶囊处于三期临床试验阶段,百济神州的BGB-290胶囊涉及卵巢癌、胃癌、乳腺癌等适应症。
从研发进度来看,百济神州BGB-290胶囊是国内本土药企中研发进度最快的PARP抑制剂,全球三期临床试验已经启动。作为对铂类一线化疗有反应的局部晚期或转移性胃癌患者的维持治疗,该研究中的药物旨在用于中国晚期胃癌和复发性卵巢癌患者的治疗。