1月8日,华邦健康发布公告称,全资子公司重庆华邦制药有限公司于近日获得国家美国食品药品监督管理局批准颁发的《药品注册批件》盐酸莫西沙星片。据悉,该产品已被列入《中国上市药品目录集》(按化学药品新注册分类批准的仿制药),视为通过一致性评价,有望参与第二批带量采购招标,采购金额超过2.7亿。
表1: 《药品注册批件》基本信息
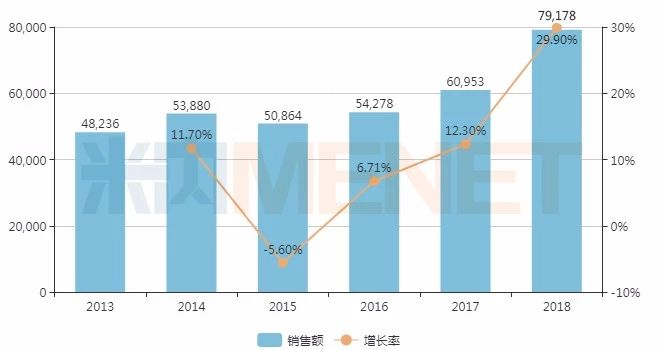
图1:全国公立医疗机构盐酸莫西沙星片销售情况(单位:万元)
据悉,盐酸莫西沙星属于第四代广谱氟喹诺酮类抗感染药。与前三代抗感染药物相比,盐酸莫西沙星对革兰氏阳性菌、革兰氏阴性菌、厌氧菌等常见致病菌的抗菌活性更强,具有安全性高、耐药性低的优点。盐酸莫西沙星主要用于治疗成人上、下呼吸道感染(如社区获得性肺炎、急性鼻窦炎、慢性支气管炎急性发作),以及皮肤和软组织感染。
在中国城市公立医院、县级公立医院、城市社区中心和乡镇卫生院(国内简称公立医疗机构),盐酸莫西沙星片销售额稳步增长,2018年达到近8亿元。目前,拜耳是市场领导者,市场份额为99.85%。
图2:之前评估过的盐酸莫西沙星片。

第二批33个带量采购品种名单于2019年12月29日正式公布,莫西沙星口服缓释剂型(0.4g)赫然在列。原研药企拜耳目前占有非常高的市场份额,国内被评估药企瓜分市场是大概率事件。随着华邦制药的进入,形成了“原研六家国内企业”的招标格局。按照规定,本轮集中采购假设原研的6家国内药企全部报名,入围企业最多可达5家。“全国有4家及以上入选企业的,按第一年协议采购额的80%计算。”如果按照最高有效申报价格折算,莫西沙星口服缓释剂型(0.4g)本次采购金额超过。