文|封丘
4月10日,CDE发布了《地舒单抗注射液生物类似药(恶性肿瘤适应症)临床试验指导原则(征求意见稿)》。意见稿从概述、临床研究策略、临床研究设计要点和总结四个方面阐述了地舒单抗注射液生物仿制药研发的总体要求。
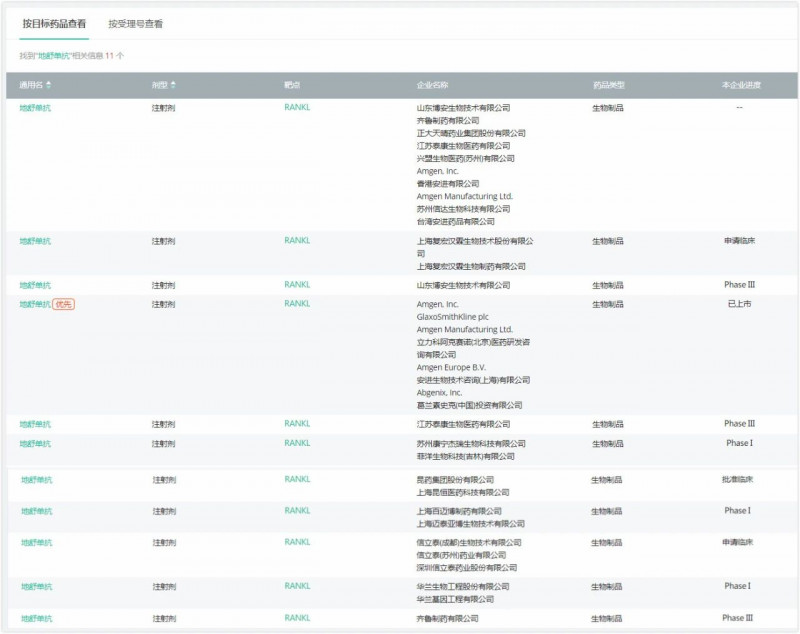
Destuzumab是在中国仓鼠卵巢中表达的人单克隆免疫球蛋白G2抗体,作用于RANK配体,抑制破骨细胞的成熟、分化和功能,减少骨吸收和破坏。该产品由美国Amgen公司开发和销售。目前国内外没有批准的地妥珠单抗生物类似物,国外也没有可供参考的单品种指导原则。目前没有相关药品申报上市。国内多家药企正在研发地舒珠单抗的生物类似物,现阶段有必要明确和统一地舒珠单抗在国内的临床试验要求。

根据PharmaGo的数据,目前齐鲁制药股份有限公司、山东博安生物科技股份有限公司、江苏泰康生物医药股份有限公司的地舒珠单抗注射液处于三期临床研究阶段;华生物、康宁杰瑞、上海百脉博药业三家公司的地舒珠单抗注射液处于I期临床研究阶段。
2019年5月21日,地舒珠单抗注射液获美国食品药品监督管理局有条件批准上市。它用于治疗患有成熟骨的成人和青少年患者,这些患者患有不能手术的骨巨细胞瘤或其手术切除可能导致严重功能障碍。地妥珠单抗可作为骨巨细胞瘤的靶向治疗,并可能成为填补该疾病未满足的医疗需求的重要治疗选择。中国临床进口注册豁免申请有境外临床数据支持,申请人提供的主要支持性临床数据均在境外获得。
