摘要
6月份,新药注册申请量继续上升,呈现上半年整体上升趋势。6月,东阳光药业带着三种新的一类药物进入CDE。科伦药业麻醉创新药首次临床仿制申请中,有19个品种没有国内批文,10个品种为目前独家品种。注射用帕瑞昔布钠和盐酸莫西沙星的模拟应用出现了趋同现象。诺华有两个新的一类药申请临床应用,深圳王海药业的二甲基丙烯酸萘替尼上半年获批临床应用,呈上升趋势。根据Minenet中MED药物评价数据库整体统计,2017年上半年新药注册申请量呈上升趋势。
从申请类型来看,6月份新药申请和仿制申请数量继续增加,仿制申请增幅较大,进口申请与上月基本持平。
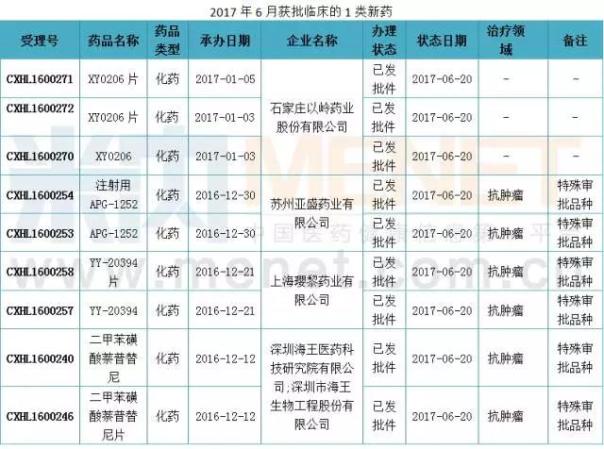
国内新药申报:东阳光3个1类新药进入CDE,科伦药业首个麻醉创新药申报临床
根据Minenet的MED药物评价数据库,2017年6月共有65个新药申请,其中一类新药申请38个,涉及13个品种。在完成临床试验阶段后,Furutinib于本月宣布生产。6月,广东省东阳光药业有限公司带着三个一类新药进入CDE,分别是利他灵及其片剂、HEC74647PA及其片剂、HEC68498钠盐及其片剂。但这三个品种的具体信息目前还没有检索到。此外,随着3月份康达韦钠和HEC30654AcOH的应用,2017年上半年东阳光有5个一类新药。下面简单介绍一下——年6月的一些新药。
Furutinib:一种高选择性的VEGFR长效抑制剂,用于治疗直肠癌、非小细胞肺癌和胃癌。和记医院拥有该药的完全自主知识产权,目前正在进行该药对晚期非小细胞肺癌适应症的临床研究。
NB001:浙江永展医药是治疗慢性疼痛的创新药物。永展医药在全球范围内拥有该药的核心专利和自主知识产权。
ZSP0391:众生药业年内申报的第二个一类新药。根据众生药业的公告,ZSP0391是众生药业自2016年以来提交临床试验注册申请的第四个具有自主知识产权的创新小分子药物。ZSP0391原料药和片剂由广东众生药业股份有限公司和上海药明康德共同研发,主要用于治疗EGFR敏感突变和T790M耐药突变的非小细胞肺癌患者。
KL100137:由科伦药业自主研发,是科伦药业在麻醉领域的首个创新药,也是继KL070002、KL-A167注射液之后,科伦药业年内进入CDE的第三个一类新药。非临床研究结果表明,KL100137通过激活GABAa受体发挥麻醉作用,具有起效快、诱导快、平稳、持续输注后无蓄积、恢复快、无明显呼吸和心血管抑制作用等特点,且麻醉过量可被马西尼逆转和抢救。其疗效和安全性优于丙泊酚和瑞马唑仑。
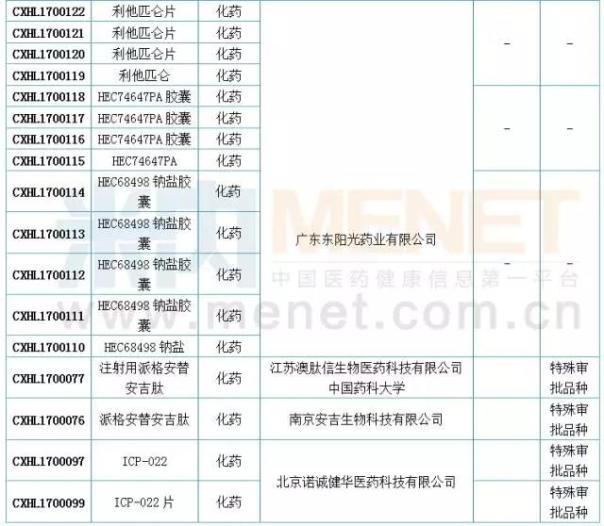
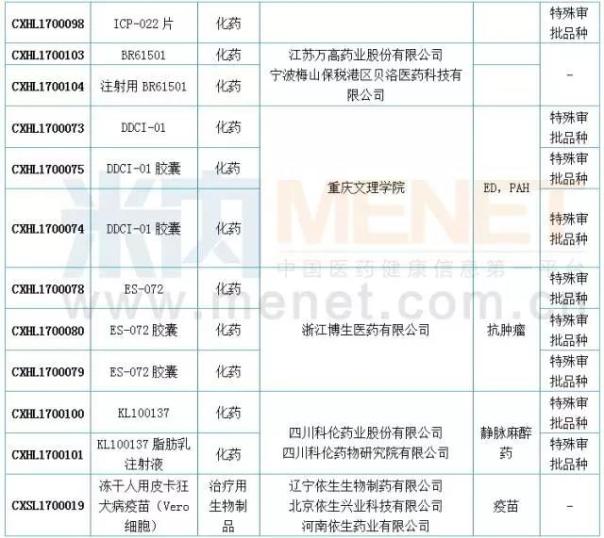
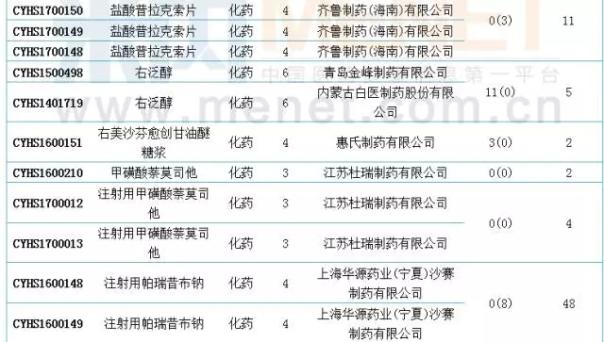
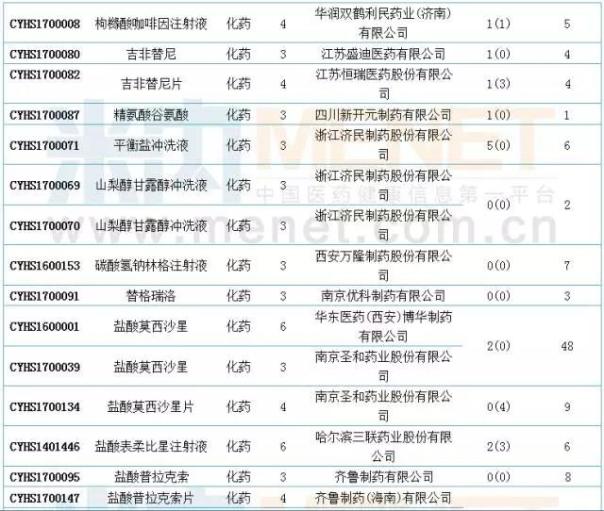
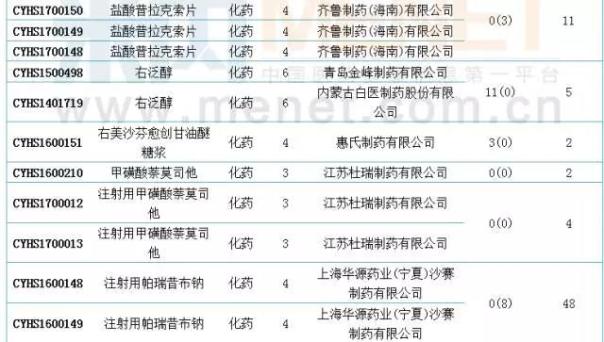
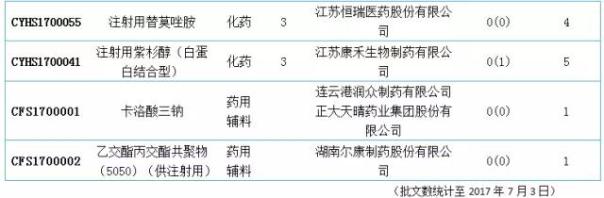
国内仿制申报:19个品种目前尚无国产批文
6月新增50款国产模仿应用。根据MINI中MID药物索引数据库的统计。com,6月份进入CDE的仿制申请中有19个品种,目前没有国内相关厂家的生产批文。此外,阿哌沙班片、恩利生坦片、达沙替尼原料药、氟比洛芬酯注射液、吉非替尼原料药、精氨酸谷氨酸原料药、盐酸莫西沙星片、盐酸普拉克索片、注射用帕瑞昔布钠、注射用紫杉醇(白蛋白结合型)等10个品种为目前国内独家品种。值得一提的是,注射用帕瑞昔布钠和盐酸莫西沙星共有48个待受理号,有扎堆申报的迹象。
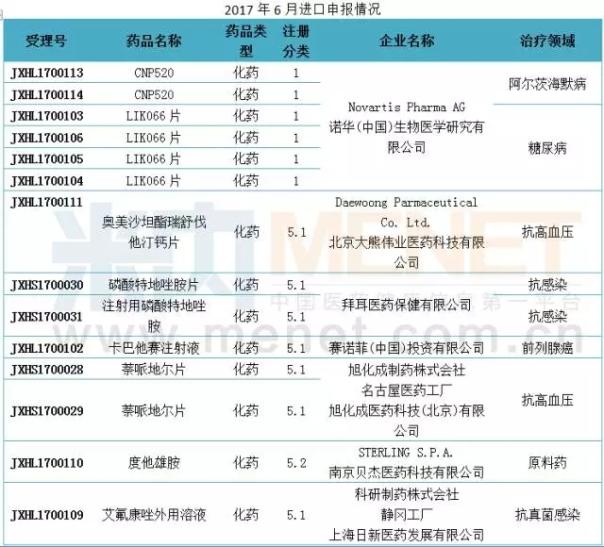
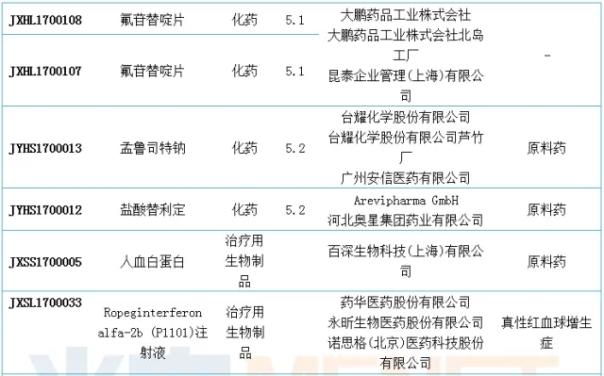
进口申报:诺华有两个1类新药申报临床
6月份,CDE新增进口申请28件,涉及18个品种,多为5个类别的申请。在……里
6月,石家庄以岭药业XY0206 API及其片剂、苏州亚圣药业APG-1252 API及其注射剂、上海英利药业YY-20394 API及其片剂、深圳王海药业二甲基丙烯酸萘普替尼API及其片剂4个一类新药获批临床。