昨天,默克(MSD)宣布,欧洲药品管理局(EMA)的人用医药产品委员会(CHMP)建议有条件批准其埃博拉疫苗Ervebo(V920),以预防埃博拉病毒在18岁及以上人群中引起的疾病。如果获得批准,Ervebo将成为世界上第一个获得批准的埃博拉疫苗。
埃博拉是一种非常罕见的病毒。它是一个通用术语,用来指属于纤维蛋白学的埃博拉病毒的一组病毒。可导致人类产生埃博拉出血热,死亡率高。死亡的主要原因是中风、心肌梗塞、低血容量性休克或多器官衰竭。在刚果的一次疫情中,超过2000人死于埃博拉病毒感染。现在,它已经成为世界上第二大流行病毒。世界卫生组织称,自2018年8月1日刚果爆发疫情以来,已有超过3000名患者被确认感染。
Ervebo由改良的水泡性口炎病毒(VSV)和埃博拉病毒表面的一种重要糖蛋白组成。VSV能使一些牲畜生病,但对人类无害。该病毒通过产生轻度感染激活免疫系统,使后者产生针对埃博拉蛋白的抗体。尽管Ervebo在美国和欧盟尚未获得批准,但由于疫情的严重性,默沙东响应了世界卫生组织(世卫组织)的要求,提供了大量的研究准备。根据不可预测和不断变化的疫情需求,默沙东已经开始准备增加对世卫组织和其他机构的Ervebo供应。
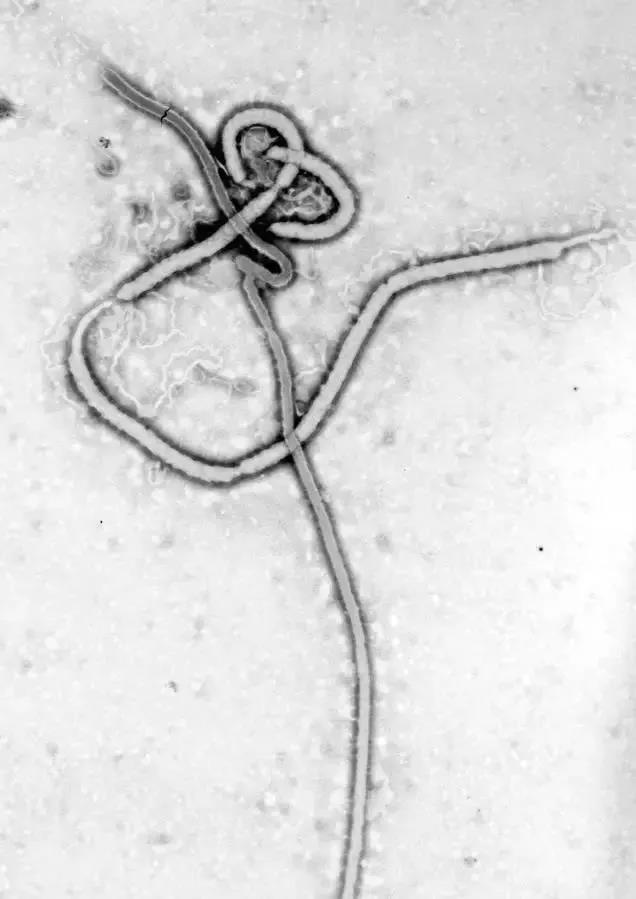
埃博拉病毒的电子显微镜图片(来源:CDC/弗雷德里克a墨菲博士[公共领域])
发表在《柳叶刀》期刊上的一项研究表明,爱尔维博可以维持两年的预防效果。与其他埃博拉疫苗相比,预防效果只能维持6个月左右。对埃尔韦博的长期保护无疑会对未来抗击埃博拉产生积极作用。此前,美国FDA已经授予Ervebo突破性疗法认定和优先审评资格,预计在明年3月14日前回复其上市申请。
默克研究实验室主席罗杰m佩尔穆特(Roger M. Perlmutter)博士说,“CHMP的建议是Ervebo保护可能受埃博拉病毒影响的人的重要一步。“我非常感谢世界卫生组织和许多其他政府和非政府组织为促进埃博拉疫苗的开发所做的不懈努力。目前,我们的当务之急是获得德国爱尔维博制造商的监管批准,从而实现后续的生产和供应,支持全球公共健康目标。”
参考资料:
[1]2019年10月18日,默克收到欧盟CHMP对用于预防埃博拉病毒疾病的试验性V920埃博拉扎伊尔疫苗的积极意见,检索自
关注药明康德微信官方账号
