11月5日,清华大学陈小元研究员和吴一龙教授在《自然评论药物发现》杂志上发表了题为《Trends in oncology drug innovation in China》的文章(IF=64.797),分析了我国癌症药物研发的创新趋势。


本文数据主要来源于pharma cube)pharma go和Next PharmaDatabase。在这里,我将这篇文章分享给大家。
以下是论文原文的翻译:
中国的制药业从未如此激动人心。如今,我国药企的研发重点已经从仿制药转向创新药,而肿瘤领域一直处于这一转变的前沿。从2018年到2020年8月,中国批准的44种癌症新药中,有12种是在中国本土研发的。虽然大部分都是市场上同类产品的跟风药,但是一流的候选药还是层出不穷。
本文总结了中国在研癌症新药的管道情况,旨在为中国医药生态系统的演变和研发趋势提供见解。
从me-too到first-in-class的转变
截至2020年1月,中国共有821种处于不同临床开发阶段的抗癌候选药物,其中包括404种me-too/me-better和359种第一类(FiC)药物。Me-too定义为与已批准上市的药物具有相同靶点和相似作用机制的药物;FiC被定义为没有任何种类的已批准药物或对同一靶点具有全新作用机制的药物。
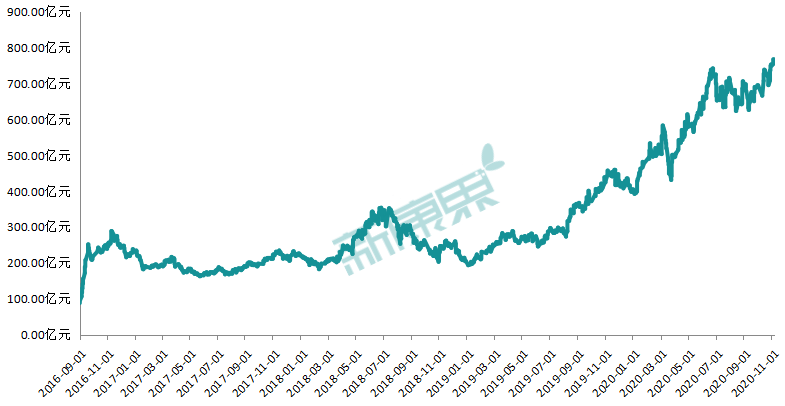
图1 |中国正在研究的抗癌药管道概况。821药物分为免疫肿瘤药物、靶向药物和细胞毒药物三大类,并根据作用靶点和作用机制分为一类和类药。由于信息不充分而无法归入3个主要类别的产品归入“其他”类别(未显示)。
国内很多初创企业出于商业生存和发展的考虑,选择了风险更低、R&D速度更快的me-too药物,包括紧跟国际前沿的细胞疗法。在me-too药物中,数量最多的类型包括56种针对CD19的CAR-T细胞疗法,83种针对EGFR或HER2的靶向疗法,以及32种PD-1/PD-L1单克隆抗体。
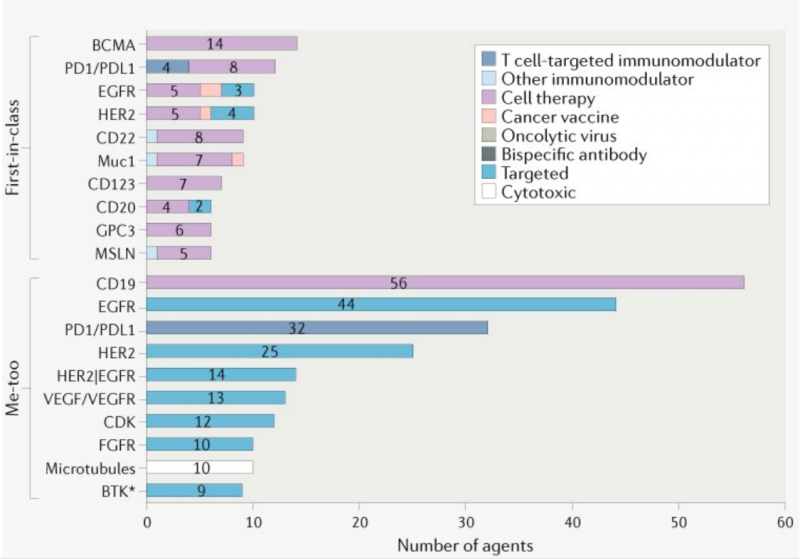
图2 | TOP10,中国一流、我也肿瘤创新药热门标的
适度的市场竞争可以提高患者用药的可及性,但只专注于开发me-too药物可能会降低资源使用效率,阻碍长期创新。随着市场日趋成熟和自我规范,有限的市场份额可能会降低me-too候选药物在同类药物激烈竞争中的吸引力。政府的政策调整,如医疗保险改革导致的利润率降低,以及监管机构对未来研发证明优于现有治疗药物的新药的上市要求,可能会进一步促进同类最佳药物的研发。在这方面,EGFR抑制剂almonertinib和BTK抑制剂zanubrutinib是最近成功的例子。
前沿科学发现和技术革命往往源于学术界。学术界研发的一流肿瘤药物比例高于产业界的数据(80% vs 40%%)可以支持这一点。然而,进一步的产品开发和商业化需要工业界的参与和合作。比如全球首个以磷脂酰肌醇蛋白聚糖3(GPC3)为靶点的CAR-T细胞疗法的研发案例,就是学术界和产业界合作的典型。
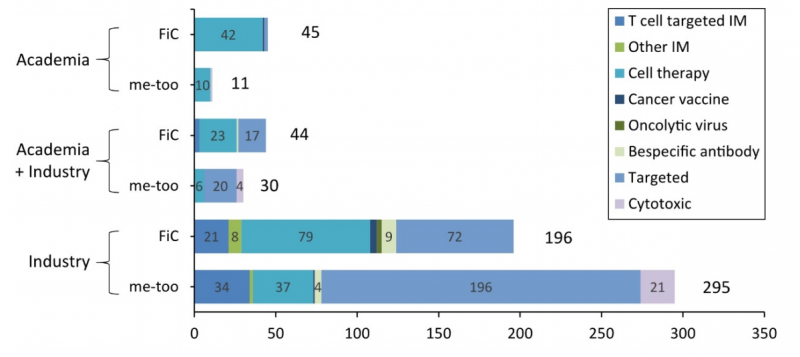
图3 |学术、产业或跨界合作发现的自研抗癌药。FiC=一流;IM=免疫调节剂。
在中国一流的产品管道中,有大量免疫肿瘤学领域的候选药物。细胞治疗尤为突出,占224种FiC IO药物的67% (150种),在FiC药物(如BCMA、CD22、CD123、GPC3)的前10个靶点中占据领先地位。这反映出,就研究数量而言,中国在全球细胞治疗领域占据优势,仅次于美国。
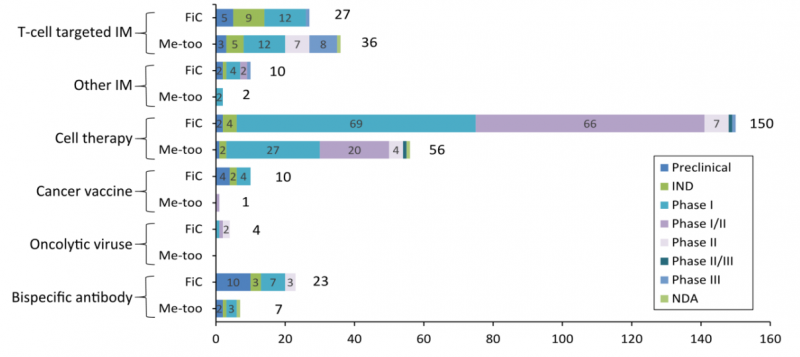
图4 |正在研发的326种免疫治疗药物概述;FiC=一流的
先进的技术为药物的发展创造了更多的可能性。技术的发展也为以新的机制作用于单个或多个靶点提供了可能,如靶向PD-1/PD-L1、EGFR和HER2的细胞治疗,基于HER2的双特异性抗体和基于CD19的双靶点细胞治疗;随着联合治疗成为癌症治疗的基石,多靶点药物可能具有转化潜力,如PD-1/CTLA4、PD-1/VEGF、PD-1/TGF-等。
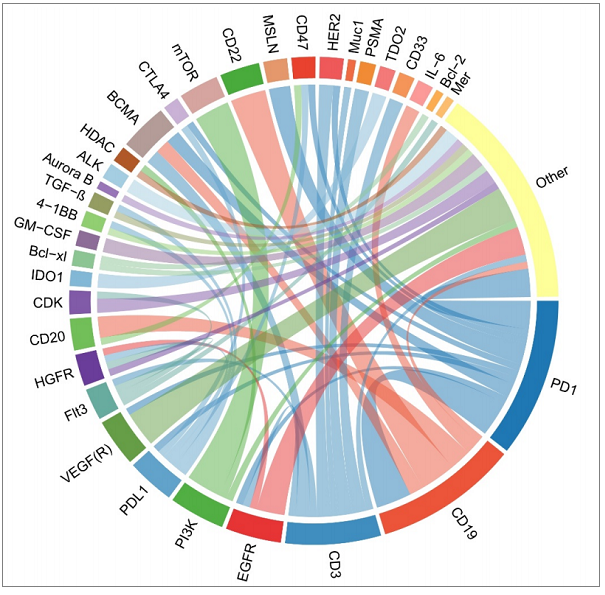
图5 |一流多靶点药物的靶点组合
需求驱动创新
开发药物是为了满足临床需要。在整个产品管道中,开发了495种用于治疗实体肿瘤的药物,其中靶向治疗占最大比例(62%)。虽然使用细胞疗法解决实体瘤存在重大挑战,但仍有83种细胞疗法正在研究中。在为血液肿瘤开发的249种产品中,细胞治疗约占一半(51%),包括CD19等验证靶点和CD22、BCMA等FiC靶点。
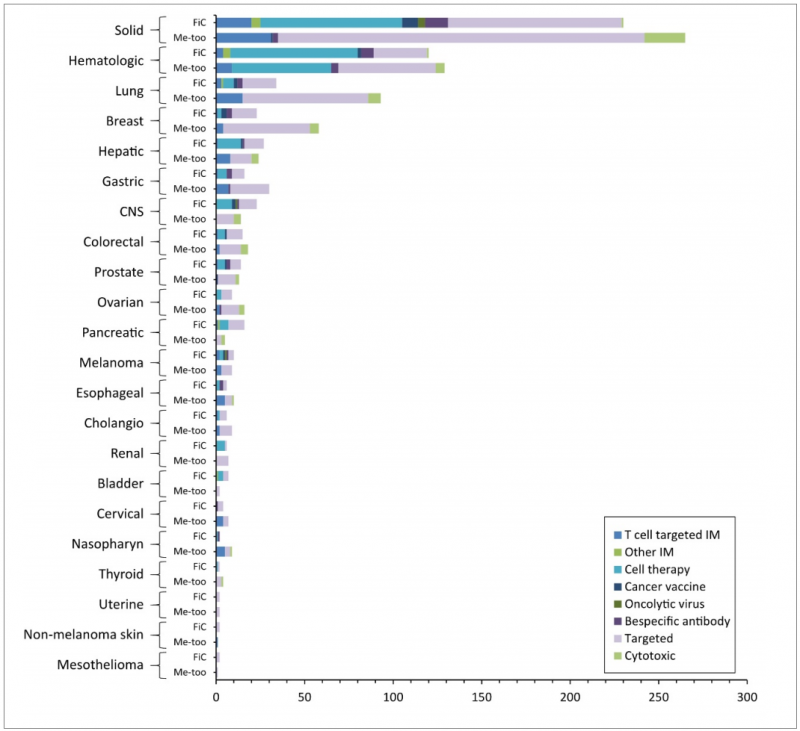
图6 |不同类型癌症研究中的药物类型概述
残疾调整生命年(DALYS)是一种疾病负担的度量,包括发病率、死亡率和残疾程度,可以粗略地反映未满足的医疗需求。分析表明,在23种实体肿瘤和7种血液肿瘤中,我国在研产品数量与相应疾病负担之间存在较强的相关性。肺癌是我国疾病负担最大的癌症,候选药物数量最多,其中大部分是跟风药物。而我国其他疾病负担较高的癌症如食管癌、胃癌、肝癌的候选药物数量低于线性相关的预期数量。肿瘤具有相对较高的一类产品比例,这可能部分是由于缺乏针对这些癌症的有效靶点,从而探索更多的新靶点和新机制。
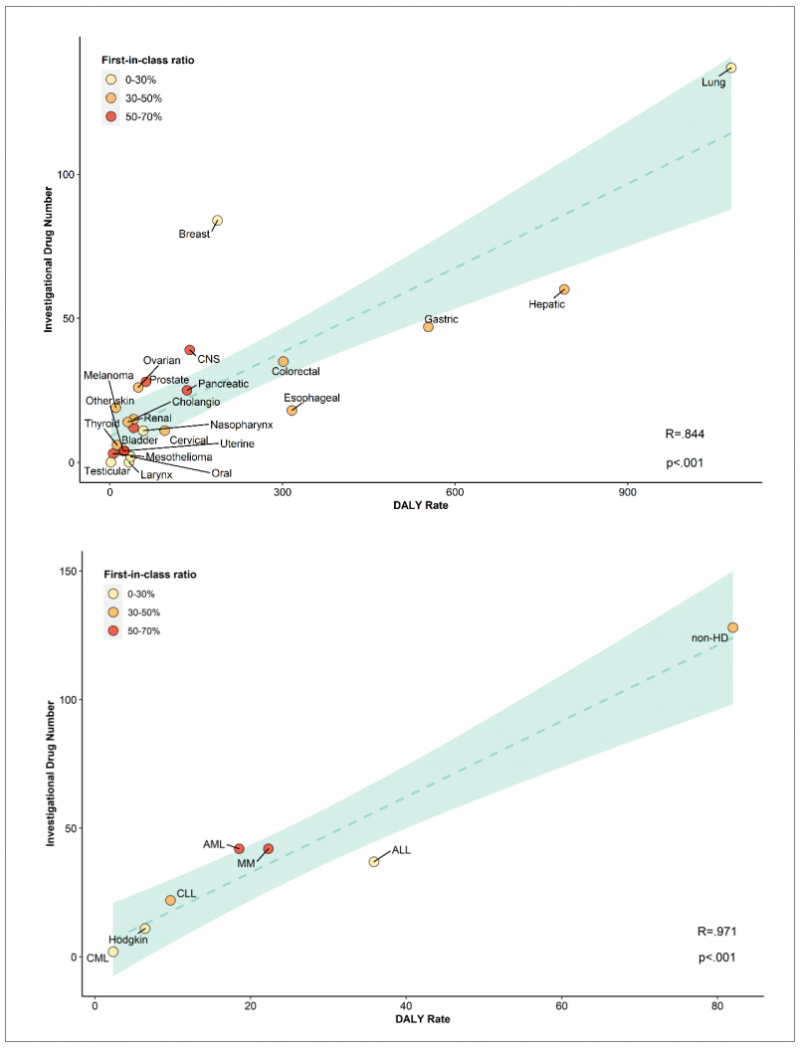
图7 | 23个实体瘤(A)和7个血液肿瘤(B)中正在开发的新药数量与DALY之间的相关性。DALY率表示使用全球疾病负担(GBD)2017年数据库()的数据计算的中国每10万人口的癌症DALY。颜色表示每种癌症类型的相似候选药物的比例,阴影虚线表示线性拟合的95%置信区间,右下角显示Pearson相关系数(R)和P值。
授权和引进
中国已成为R&D全球化的主要目标国家。对于外国公司,尤其是生物技术公司来说,进入中国市场的一种方式是向中国生物制药公司发放许可证。到2020年初,从国外获得许可的候选产品在中国癌症产品整个管道中的比例已增加到18% (147),主要发生在临床前或临床早期。典型的路径是先选择小适应症或晚期肿瘤作为发展目标,可能会缩短进入中国市场的时间。例如,尼拉帕利在2016年获得Tesaro的许可,2019年在中国获得复发性卵巢癌的市场批准。值得注意的是,境内外同步阶段的产品有30个,凸显了中国接受海外数据的开放态度。
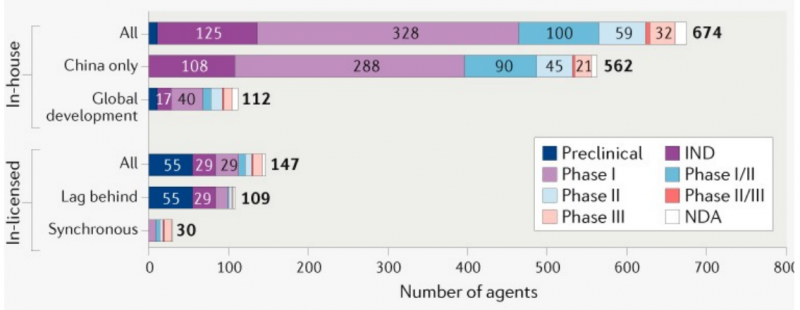
图8 |国内外自主研发和进口产品发展状况
自主开发的产品分为仅在中国开发的产品和在中国及其他国家开发的产品。进口产品基于中外最新发展阶段对比,包括晚于其他国家,或与其他国家同步;另外8段缺乏相关信息,无法归类。
中国自主研发的创新药物产品越来越多地在全球范围内开发(674种药物中的112种,如上图所示),这表明海外国家已经认可了中国的R&D能力、制造质量和研究设计。特别是17种药物已经授权给海外公司。例如,南京联想公司针对BCMA的CAR-T细胞疗法LCAR-B38M分别在美国和中国被认定为突破性疗法,让桑生物技术公司于2017年获得授权。
展望
虽然中国创新肿瘤产品的研发受到未满足的医疗需求的推动,但不适当的实验设计、过高的费用和不足的回报可能会阻碍创新。未来的癌症临床试验需要更具创新性的整合平台,例如在特定患者群体中测试几种候选药物,从而更有效地利用资源。如果中国继续发展鼓励创新的环境,监管机构对新技术和新产品保持开放的态度,国内外学术界和工业界建立更广泛的合作,可以预测将出现一批本土突破性疗法。
